จากการทำงาน “แบบตั้งรับ” ในคลินิกเอกชน เป็นระยะเวลา 24 ปี
ระยะเวลาที่ยาวนานเกิน 20 ปี ทำให้ผมได้เห็นภาพที่ต่อเนื่อง จากคนไข้ทั้งประจำ และ ไม่ประจำ (ได้แก่ คนไข้ที่มาบ้างนานๆ ครั้ง และ คนไข้ที่พบกันแค่ครั้งเดียว หรือ 2 ครั้ง)
ถ้านับคนไข้ที่พบกัน เมื่อ 20 ปีที่แล้ว เป็นคนอายุ 40 ปี ในปีนี้ คนไข้จะอายุ 60 ปี เข้าคำจำกัดความผู้สูงอายุไปทันที
ในช่วงที่ผ่านมา เราจะเริ่มได้ยินคำว่า “สังคมผู้สูงอายุอย่างสมบูรณ์”
สังคมผู้สูงอายุอย่างสมบูรณ์ หมายความว่า ตั้งแต่ปีที่แล้ว (พ.ศ. 2566)
เวลาเดินตลาดเจอคนไทย 10 คน จะพบ ผู้สูงอายุ 2 ท่าน
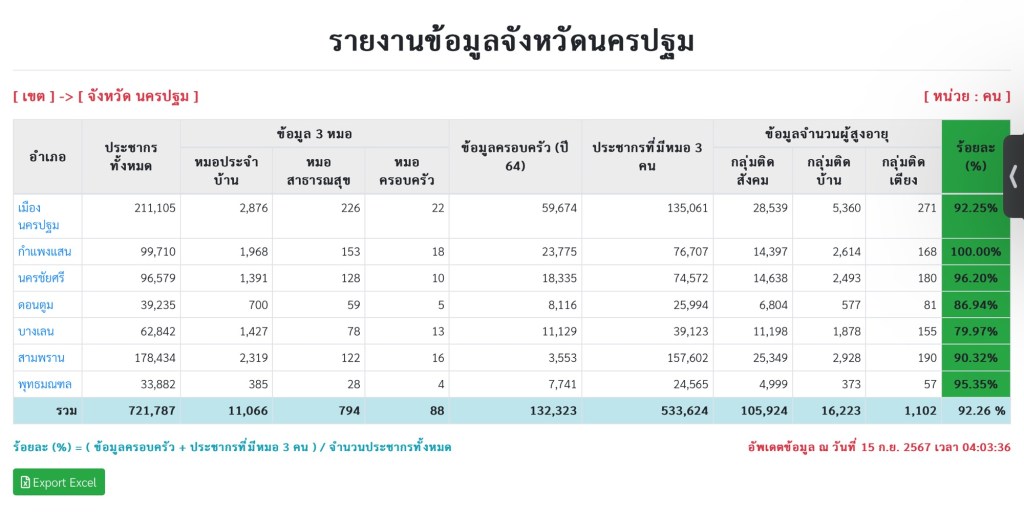
จากรูป ถึงแม้ภาคกลางจะมีจำนวนผู้สูงอายุ มากที่สุด (คือ มากกว่าทุกภาค)
แต่สำหรับจังหวัดนครปฐม ถ้าดูตัวเลขแล้ว ภาพรวมของทั้งจังหวัด และ ใน อ.เมือง ตัวเลข ผู้สูงอายุ / จำนวนประชากรทั้งหมด ตัวเลขจำง่ายๆ อยู่ที่ 17 % ครับ
ข้อมูลล่าสุด ณ ปีนี้ พ.ศ. 2567
และจาก การสำรวจของ กระทรวงสาธารณสุข ตามตารางนี้นะครับ
ผมขอใช้เป็น “ต้นแบบ” ในการแบ่งกลุ่ม การดูแลสุขภาพช่องปากและฟัน ตามแนวทางนี้เลย
ผู้สูงอายุในกลุ่มติดสังคม และ กลุ่มติดบ้าน ถือ เป็นกลุ่มที่มีความเสี่ยงต่อ การเกิดโรคในช่องปากต่ำ – ปานกลาง (ในกลุ่มนี้มีโอกาสเกิดความเสี่ยงสูง อยู่ด้วย ขึ้นกับ พฤติกรรมการใช้ชีวิต เช่น อาหารที่ชอบกิน, เครื่องดื่มที่ชอบดื่ม, ความบ่อยในการกินอาหาร หรือ นิสัยอื่นๆ ที่ไม่เกี่ยวกับการกิน เช่น การสูบบุหรี่ เป็นต้น)
ส่วนผู้สูงอายุในกลุ่มติดเตียง ถือว่า เป็นกลุ่มที่มีความเสี่ยงสูง ถ้าติดเตียงโดยมีองค์ประกอบร่วม คือ
เป็นผู้สูงอายุที่ยังมีฟันธรรมชาติ
เป็นผู้สูงอายุที่ยังมีฟันธรรมชาติ และยังใช้ฟันปลอมร่วมด้วย (อาจจะเป็นแบบติดแน่น หรือ ฟันปลอมแบบถอดได้)
ผู้สูงอายุที่ไม่มีฟันธรรมชาติเลย และยังใช้ฟันปลอมทั้งปากอยู่
การดูแลที่ต่างกัน ความแตกต่างนั้นมีอยู่ปัจจัยเดียว คือ ความสามารถในการแปรงฟัน ดูแล ด้วยมือของตัวเองได้ กับ ต้องมีผู้ช่วยเหลือ คอยดูแล นั่นเองครับ
ตอนนี้จะพูดถึงในกลุ่มแรกก่อน คือ ผู้สูงอายุที่ดูแลตัวเองได้ครับ
โดยทั่วไป เรารู้ว่า ควรแปรงฟันวันละ 2 ครั้ง แต่สิ่งที่รู้กันน้อยมาก คือ เราควรแปรงฟันกัน ครั้งละนานกี่นาที ?
เรารู้ว่า ยาสีฟันมี ฟลูออไรด์ และต้องการแปรงฟันให้ ฟลูออไรด์ในยาสีฟัน ซึมเข้าไปในผิวฟัน เพื่อป้องกันไม่ให้ฟันผุ
ถ้าเราลองดูตัวเลข เวลาที่หมอฟัน ทายาที่เป็นฟลูออไรด์ชนิดเข้มข้นบนผิวฟัน ความเข้มข้นที่ใช้ทาของยา จะมี ฟลูออไรด์ ~ 10,000-20,000 ppm ใช้เวลาทานาน ~ 2-4 นาที
ทีนี้ ยาสีฟันสูตรทั่วไปที่ใช้กันจะมี ปริมาณฟลูออไรด์ ~ 1,500 ppm ( มากที่สุดที่หาซื้อในทั่วไป)
ระหว่าง ยาฟลูออไรด์ กับ ยาสีฟัน ที่ใช้กันตามบ้าน จะมีปริมาณ ฟลูออไรด์ ต่างกัน = 15,000/1,500 = 10 เท่า
นั่นหมายความว่า ถ้าให้ได้ผลป้องกันฟันผุได้ดี ใกล้ๆ กัน เราต้องให้ยาสีฟันสัมผัสฟัน นาน = 3 x 10 = 30 นาที
ซึ่งเป็นตัวเลขที่แปลกประหลาดมาก ถ้าจะมีคำแนะนำให้แปรงฟันถึง 30 นาที
แต่ก็เป็นไปแล้วในปัจจุบันครับ และตัวเลขนั้นมากกว่า 30 นาที ขึ้นไปอีก
(เป็นเอกสารจาก สำนักงานทันตสาธารณสุช กรมอนามัย สธ ที่ได้ไปค้นคว้ามาอีกที)
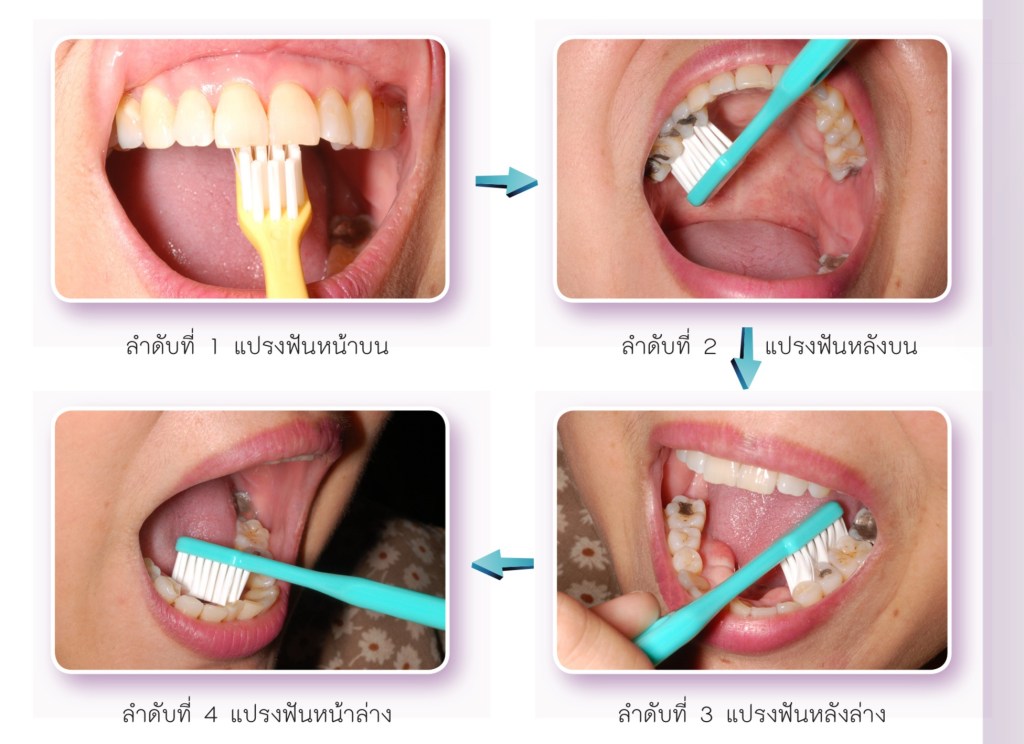
สำหรับวิธีการแปรงฟัน ปัจจุบัน จะใช้คำแนะนำให้ขยับแปรงสั้นๆ หรือ หมุนแปรงเป็นวงกลม วนไปมา โดยให้ตำแหน่งขนแปรงอยู่ใกล้ๆ ขอบเหงือก ถือเป็นวิธีที่มีประสิทธิภาพสูงสุดครับ
ref:
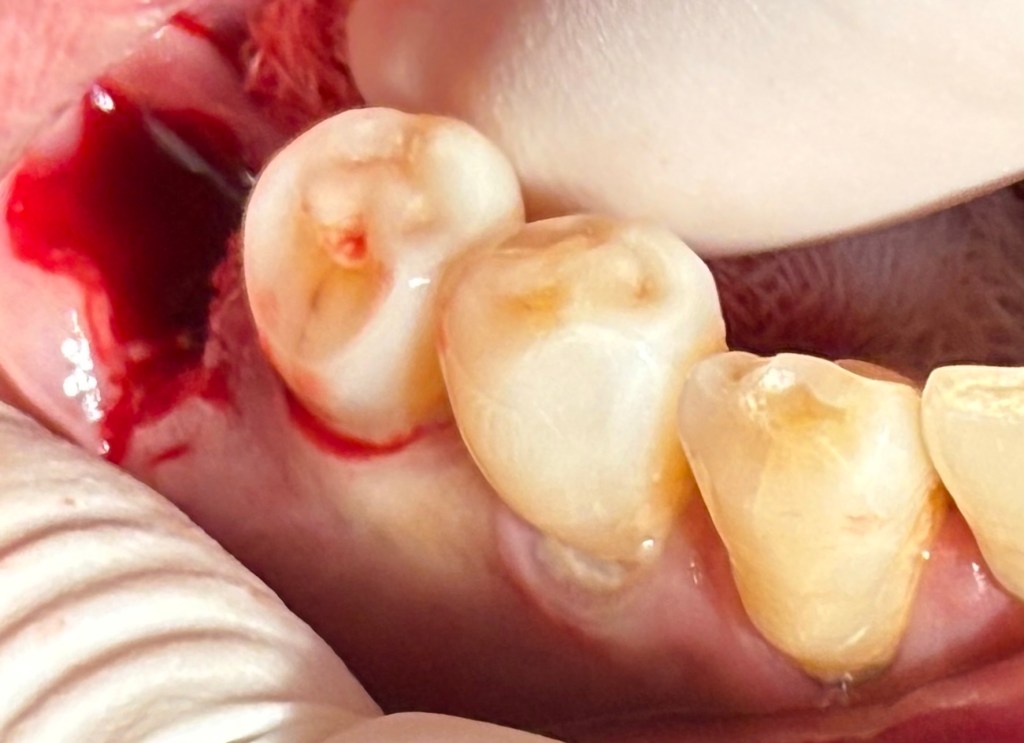
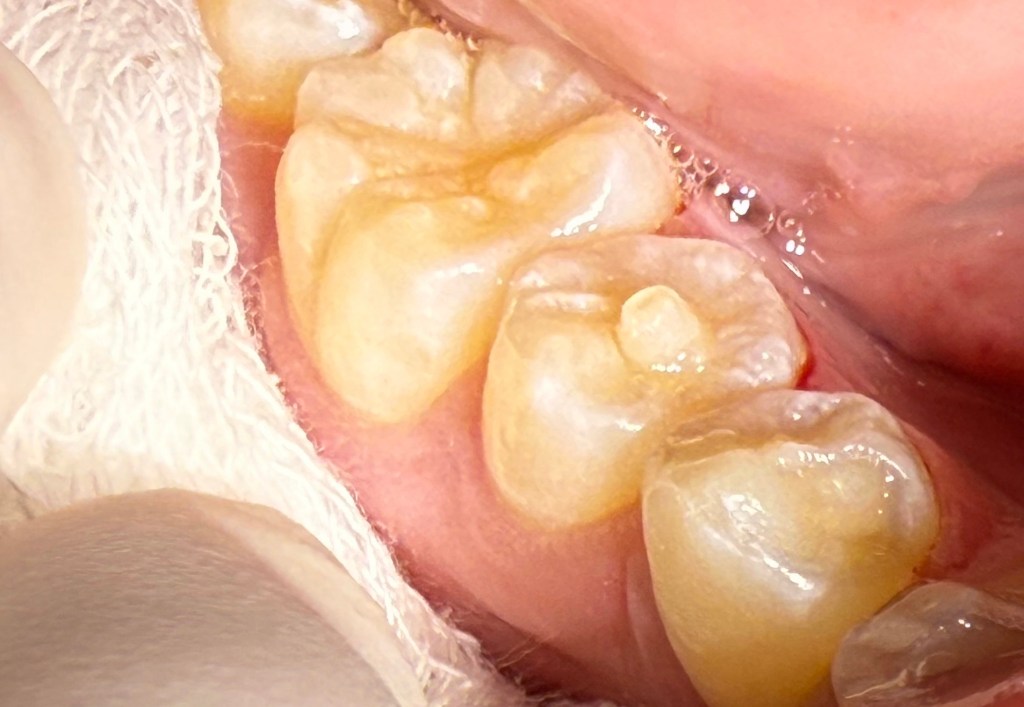
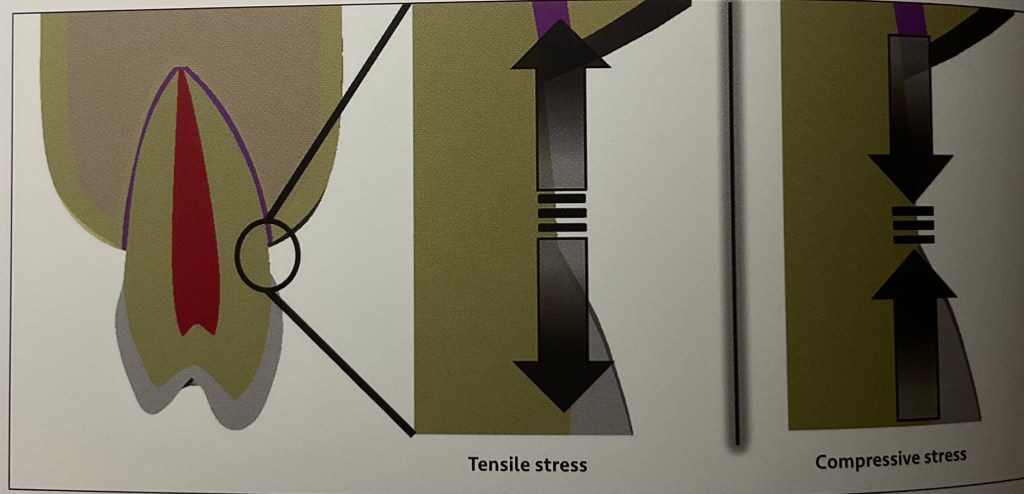
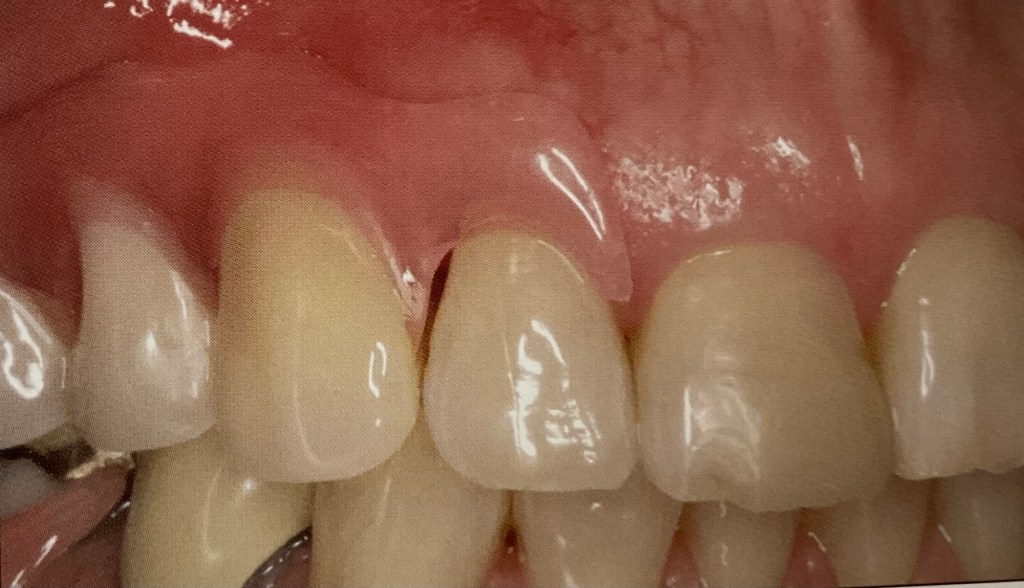
การขยับแปรงเพียงจังหวะ “สั้นๆ” หรือ หมุนเป็นวงกลม (วงรี ก็ได้) จุดประสงค์ที่แฝงไว้คือ เป็นการไม่ทำให้เกิดฟันสึก ครับ โดยเฉพาะในส่วนของฟันที่ง่ายต่อการสึกมากที่สุด ตามตำแหน่งในรูปนี้ครับ
เรื่องนี้ ขอขยายอีกนิด ในมุมของหมอฟันปลอมครับ
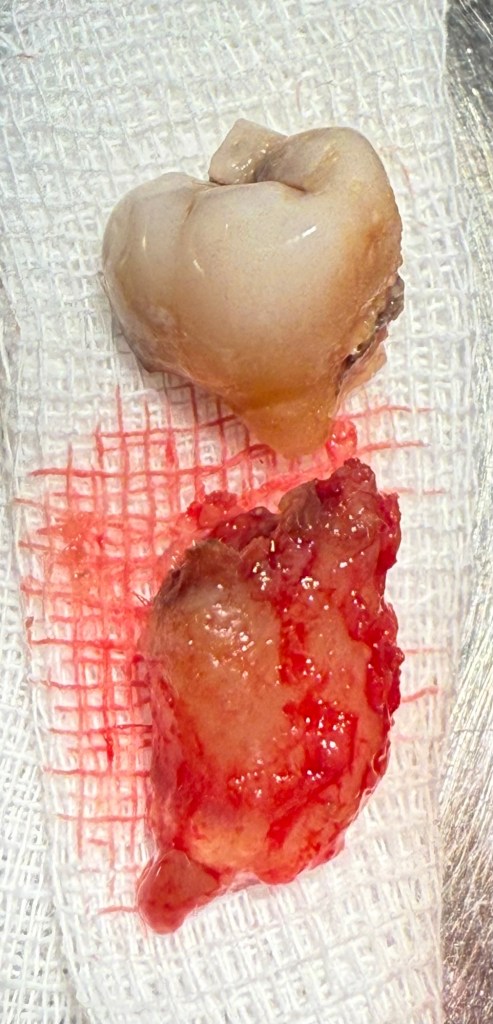
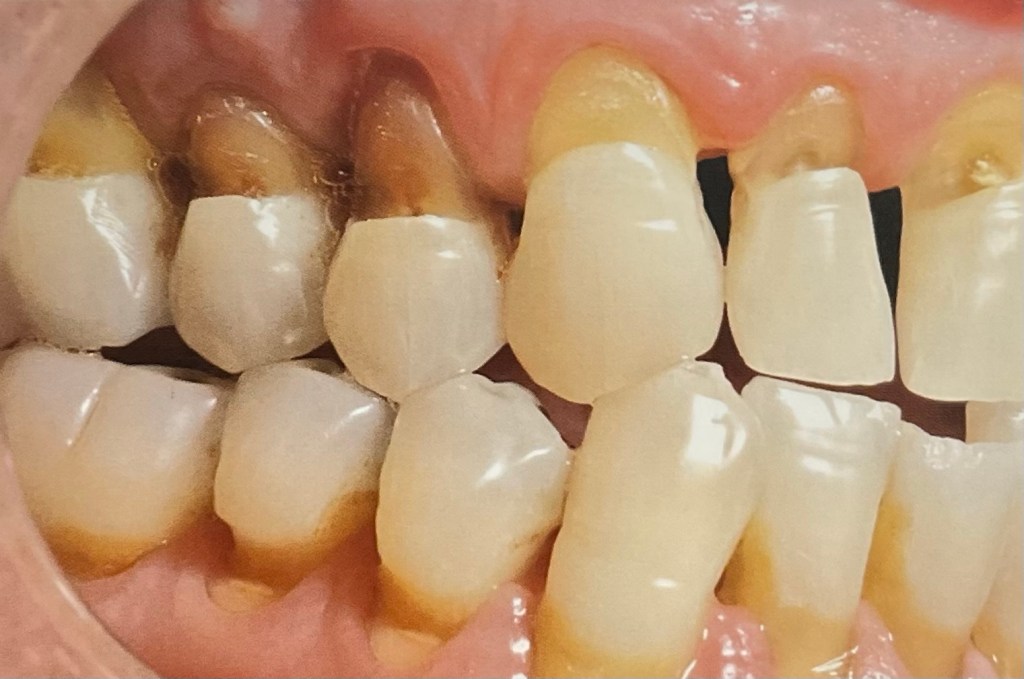
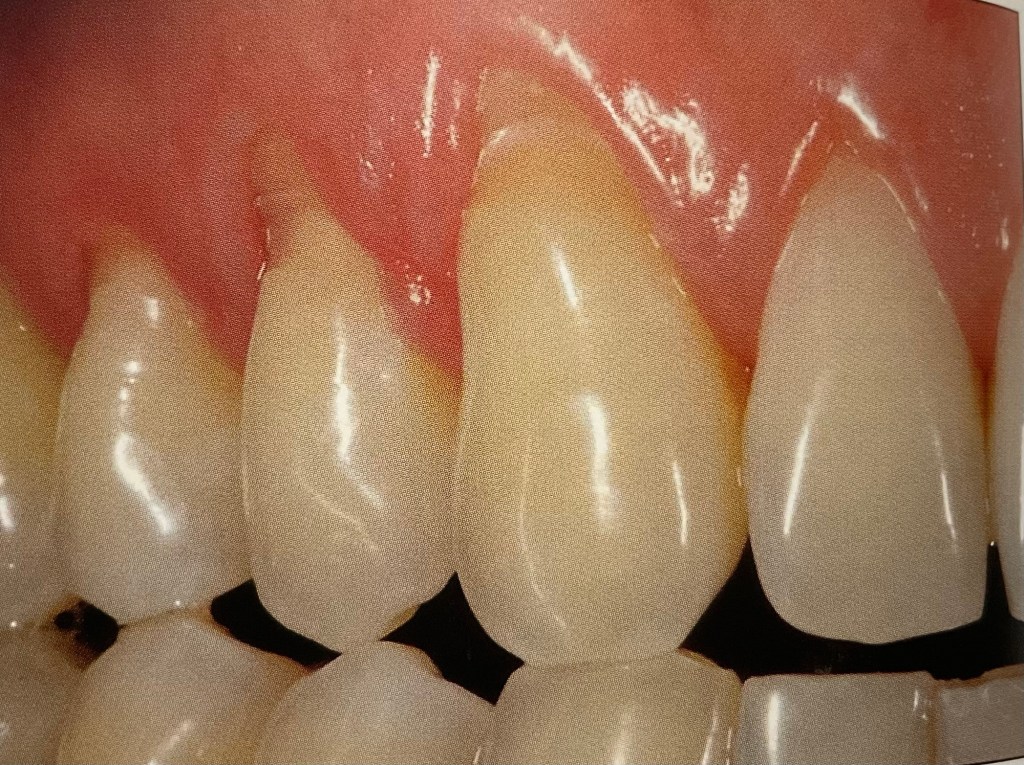
คือ แม้ในการตรวจของหมอฟัน ก็ยังมีหมอที่เห็นคนไข้ที่มีลักษณะแบบนี้ แล้วต้องถามต่อว่า “ใช้แปรงที่มีขนแปรงแข็ง มั๊ยครับ?”
แต่ประวัติจริงๆ ของคนไข้คนนี้ คือ เขาไม่ได้ใช้การแปรงฟันด้วย แปรงสีฟัน และ ยาสีฟัน ครับ แต่ให้ประวัติคือ ชอบกินส้มมาก และกินวันละหลายลูก
การสึกที่คอฟัน ในรูปนี้เกิดการการกัดฟัน และกรดจากน้ำผลไม้ คือ น้ำสัมครับ
สำหรับคนไทย แหล่งของกรดจากอาหาร นอกจากน้ำผลไม้มาจากกรดที่มาจากผลไม้ เช่น มะนาว และ น้ำส้มสายชู ที่อยู่ในเครื่องปรุงอาหาร และ กรดในน้ำอัดลมครับ
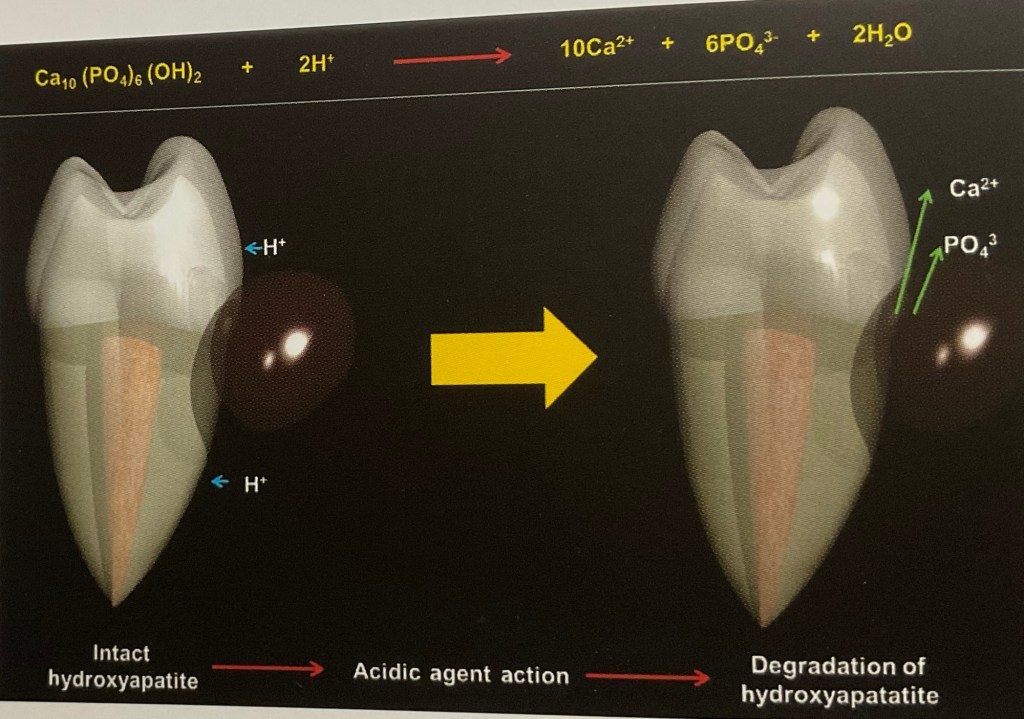
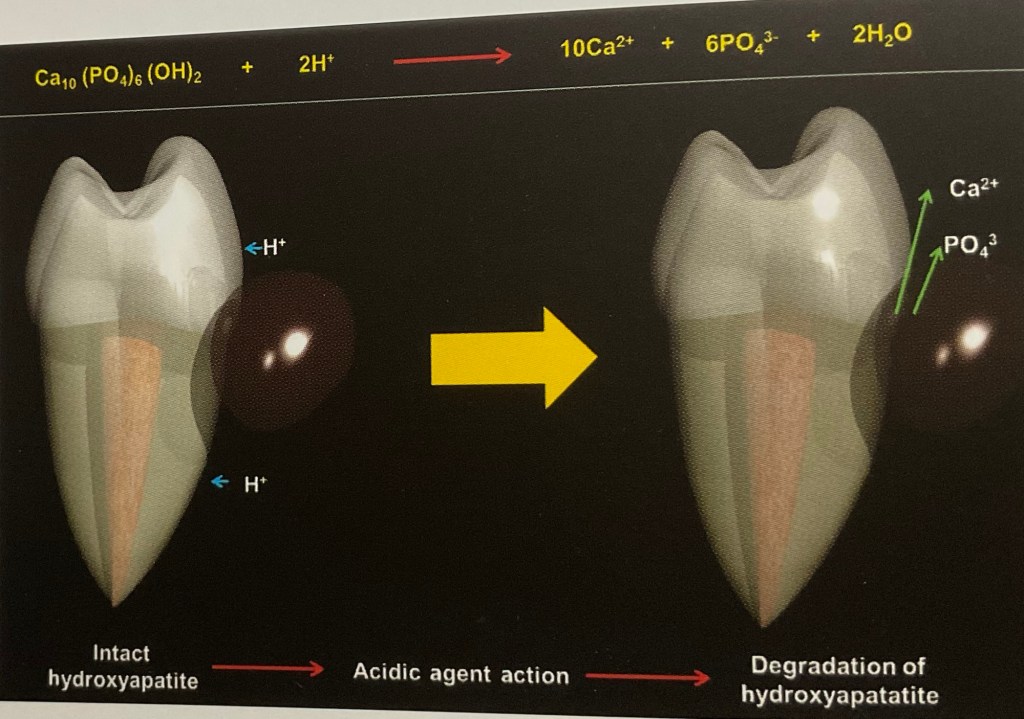
วิธีการที่กรดเข้าไปทำลายผิวฟัน
คือ การละลาย แคลเซียม และ ฟอสเฟต ที่ผิวฟัน และ เนื้อฟัน
ปัจจุบัน ความรู้ทางทันตแพทย์สมัยใหม่ เริ่มให้น้ำหนักเรื่อง ขนแปรงที่แข็ง แล้วทำให้ฟันสึก น้อยมากครับ
เพราะแปรงสีฟันที่ได้มาตรฐาน ผ่านการรับรองคุณภาพทั้งจาก สคบ. และ กรมอนามัย สธ. ไม่มีแปรงขนแข็งแล้วครับ มีเพียง ชนิด Soft และ Ultra-Soft คือ นุ่ม กับ นุ่มที่สุด
โอกาสที่ขนแปรงจะทำอันตรายจากผิวฟันน้อยมาก
ตรารับรองจาก กรมอนามัย
ตอนนี้สาเหตุหลักที่ทำให้ฟันสึก เราเชื่อ อยู่ 2 เรื่องใหญ่ๆ
คือ รูปแบบการกัดฟันของคนไข้ กับ กรดจากอาหาร เป็นหลัก
(ส่วน ความแข็งของขนแปรง และ วิธีแปรงฟันที่ผิดวิธี เช่น การขยับแปรงแบบลากยาว เป็นปัจจัยร่วมที่ทำให้ การสึกของฟันรุนแรงขึ้น เท่านั้น แต่ไม่ถือเป็นสาเหตุหลักที่ทำให้เกิด)
ในรูปแสดงตำแหน่งฟัน เวลาเราเคี้ยว
ต่อเนื่องจาก อาหารที่มีกรดผสมอยู่ เราคงไม่แยกว่า อาหารชนิดไหน มีความเป็นกรดสูง หรือ ต่ำ นะครับ เพราะ อาหารไทยที่ไม่มีส่วนประกอบของน้ำส้มสายชู หรือ น้ำมะนาว คงยากมาก แต่ถ้าคิดซะว่า อาหารที่กินมีความเป็นกรดอยู่ไม่มากก็น้อย การแปรงฟัน “ทันที” หลังกินอาหาร จึงไม่ถือว่าดีนัก
เพราะจากรูปนี้ครับ
ถ้ามีกรดจากน้ำส้มสายชู ยังคงทำงานอยู่ในปาก เราควรให้พ้นช่วงเวลานี้ไปก่อน เป็นชั่วโมงเลยก็ได้ครับ แล้วจึงค่อยแปรงฟันได้ตามปกติ
โดยส่วนตัว ผมจะไม่มีแปรงฟันหลังมื้ออาหารครับ แต่จะบ้วนปากด้วยน้ำเปล่า หลายๆ ครั้ง แล้วตามด้วยการใช้เพียง ไหมขัดฟันทำความสะอาดบริเวณซอกฟัน เพื่อขจัดเศษอาหารที่ติดออก แล้วบ้วนน้ำเปล่าตามอีกรอบ 2 รอบ เท่านั้น
ไหมขัดฟัน เลือกแบบที่ถนัดมือนะครับ บางท่านอาจจะถนัดพกแบบเป็นตลับเล็กๆ แล้วดึงมาใช้เป็นเส้น อย่างผมถนัดแบบมีก้านจับครับ (เคยให้คนไข้ลองใช้ บางท่านบอก ไม่ค่อยชอบ ถนัดแบบดึงมาใช้พันนิ้ว แบบเป็นเส้นมากกว่า)
รูปเทียบขนาดด้ามจับ กับ ดินสอดำธรรมดา
ส่วนของชนิดของยาสีฟัน และ น้ำยาบ้วนปาก ผมแนะนำให้เลือกใช้ชนิดที่ชอบในรสชาติครับ เพราะส่วนผสมทำมาแข่งกัน คุณภาพการใช้งานไม่ค่อยต่างกันตามชนิดที่มีขาย แต่ความสำคัญของการชอบใช้ เป็นเรื่องสำคัญกว่า
เพราะถ้ารู้สึกชอบในรสชาติของยี่ห้อใด ก็จะดึงดูดทำให้รู้สึกมีความสุขเวลาแปรงฟันมากขึ้นครับ ทำให้รู้สึกอยากมีเวลาแปรงได้นาน และดึงดูดให้อยากทำอย่างสม่ำเสมอครับ
ในส่วนของ ยาสีฟันชนิดพิเศษ เช่น ชนิดลดอาการเสียวฟัน สามารถซื้อมาใช้ได้อย่างปลอดภัยครับ แต่ต้องคิดว่า เป็นการลดอาการแบบไม่ถาวร และควรหาสาเหตุว่า ความผิดปกติอะไรที่ทำให้เกิดอาการเสียวฟัน หลังไปตรวจ และหมอวินิจฉัยได้แล้ว จะแก้ปัญหาได้ตรงจุดที่สุดครับ ( ok หมออาจแนะนำให้ใช้ยาสีฟันเพื่อลดอาการต่อได้ อย่างสบายใจ โดยไม่ต้องมีการรักษาอย่างอื่นเพิ่มอีก)
อีกตัวคือ ยาสีฟันชนิดทำให้ฟันขาว สามารถซื้อมาใช้ได้ อย่างปลอดภัยครับ
โดยรวมเมื่อต้องเปลี่ยนยาสีฟัน หรือ ลองซื้อยาสีฟันยี่ห้อใหม่มาใช้ ให้คิดเหมือนเราต้องใช้ยาตัวใหม่ๆ ครับ (จริงๆ ยาสีฟัน ไม่จัดอยู่ในยา แต่อยู่ในกลุ่มเครื่องสำอางค์ครับ) ถ้าลองใช้แล้ว มีอาการผิดปกติ เช่น ใช้แล้วอยู่ดีๆ หลังใช้ ปากเป็นแผล หรือ แปรงแล้วรู้สึกเสียวฟันหลังใช้ ให้ “หยุด” การใช้งานไว้ก่อน แล้วลอง “เปลี่ยน” ไปใช้ตัวเก่าที่เคยใช้แล้วไม่มีปัญหาครับ เป็นวิธีที่ง่ายสุดในการหยุดอาการที่อาจลุกลาม หรือ เป็นมากขึ้น
ต่อมา ในกลุ่มผู้สูงอายุที่ติดเตียง หรือ ต้องมีผู้ช่วยดูแล
หลักการ คือ ” ต้องมีความยืดหยุ่น ” ครับ
ยืดหยุ่นได้ทุกอย่าง เช่น ไม่จำเป็นต้องแปรงฟันให้วันละ 2 ครั้งครับ ถ้าสะดวก 1 ครั้ง และทำได้ดีพอ ก็ทำได้
หรือ จะไม่ใช้แปรง แต่ใช้ผ้าก๊อซ หรือ ฟองน้ำชิ้นเล็กๆ ชุบยาสีฟัน เช็ดและถู แบบนี้ก็ได้
อาจต้องยืดหยุ่นเวลาแปรง ไม่จำเป็นต้องเป็น เช้า หรือ ก่อนนอน ก็ได้
เช่น ถ้าผู้ดูแลสะดวกช่วงบ่าย หลังมื้อกลางวัน ก็แปรงให่้ตอนบ่ายได้ครับ
เพียงแต่ ขั้นตอนการแปรงฟันใน ผู้สูงอายุ ที่ติดเตียง ต้องมีอุปกรณ์พิเศษเพิ่มเข้ามา เช่น หลอดฉีดยาขนาดใหญ่ที่ใช้ดูดน้ำสะอาด เข้าไปฉีดล้างให้ในปาก, ตัวดูดน้ำลาย ในคนที่มีปัญหากลืนลำบาก เพื่อป้องกันการสำลัก, ถาดรองข้างเตียง เพื่อซับน้ำลายและเศษอาหาร, แปรงสีฟันไฟฟ้า ข้อดีคือ มีหัวกลมขนาดเล็ก สอดเข้าในช่องปากได้ง่าย และผ่อนแรง ผู้ดูแลไม่ต้องขยับมือแปรงฟันให้ เป็นต้น
ในส่วนของการดูแลฟันปลอม
ฟันปลอมแบบติดแน่น เพราะส่วนประกอบของฟันปลอมติดแน่น จะทำงานวัสดุ 2 ชนิด คือ โลหะผสม กลุ่มที่ไม่เกิดสนิม หรือ ไม่เกิดการกัดกร่อน กับ วัสดุอีกชนิด คือ กระเบื้อง
การยึดของฟันปลอมชนิดติดแน่น จะประสานด้วยกาว ยึดติดไปกับฟันจริง เพราะฉะนั้น การแปรงฟัน เพื่อทำความสะอาดฟันธรรมชาติ จึงเหมือนการทำความสะอาดฟันปลอมติดแน่นไปด้วยในคราวเดียวกัน
สามารถใช้ยาสีฟัน, น้ำยาบ้วนปาก และแปรงสีฟัน, ไหมขัดฟัน ทุกชนิด ได้ตามปกติ
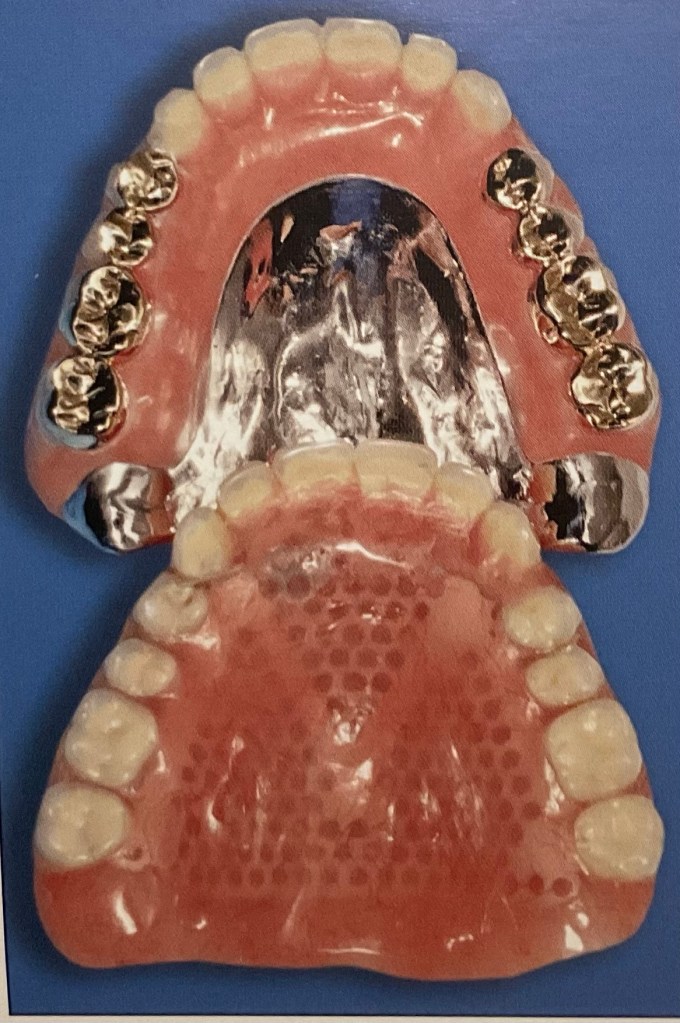
แต่ในส่วนของฟันปลอมชนิดถอดได้ ส่วนประกอบจะแบ่งออกเป็น 2 ส่วน คือ ส่วนที่เป็น อะคริลิค กับ ส่วนที่เป็น โลหะผสม
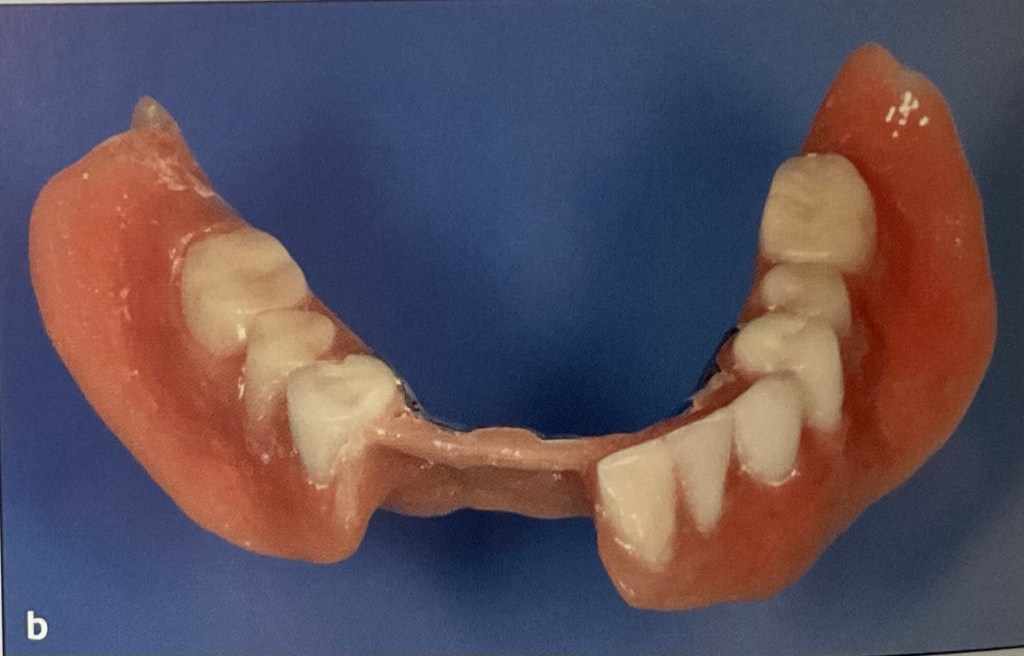
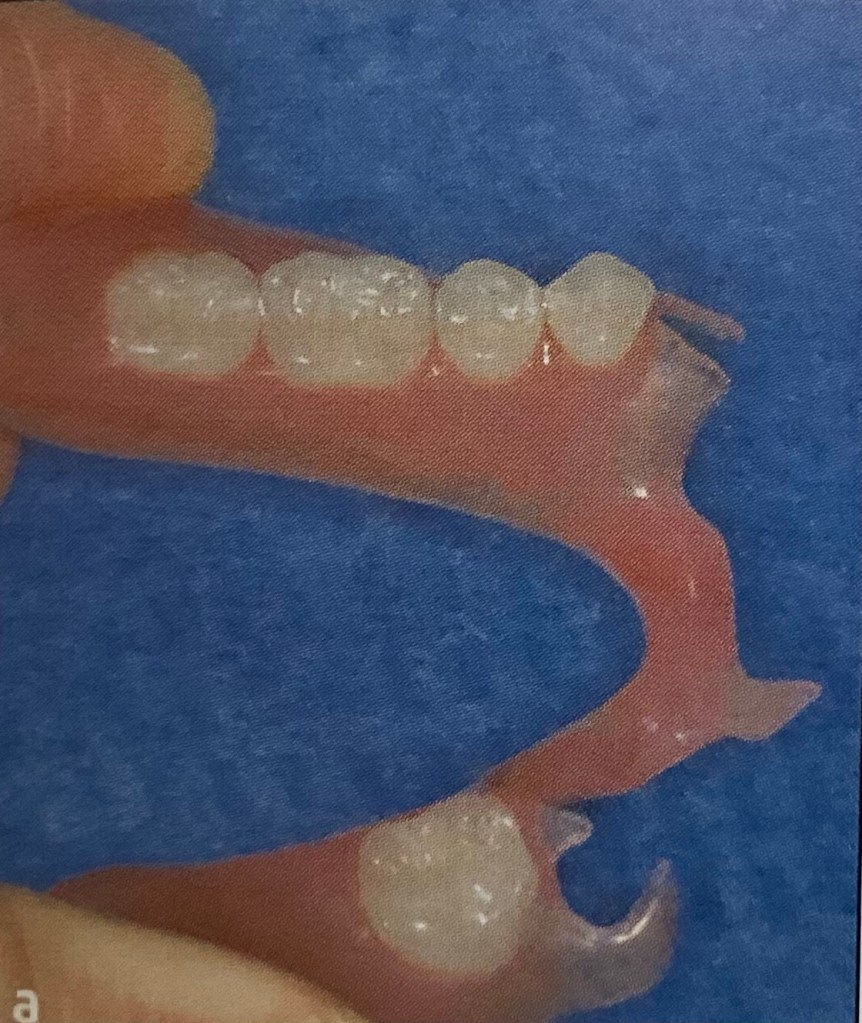
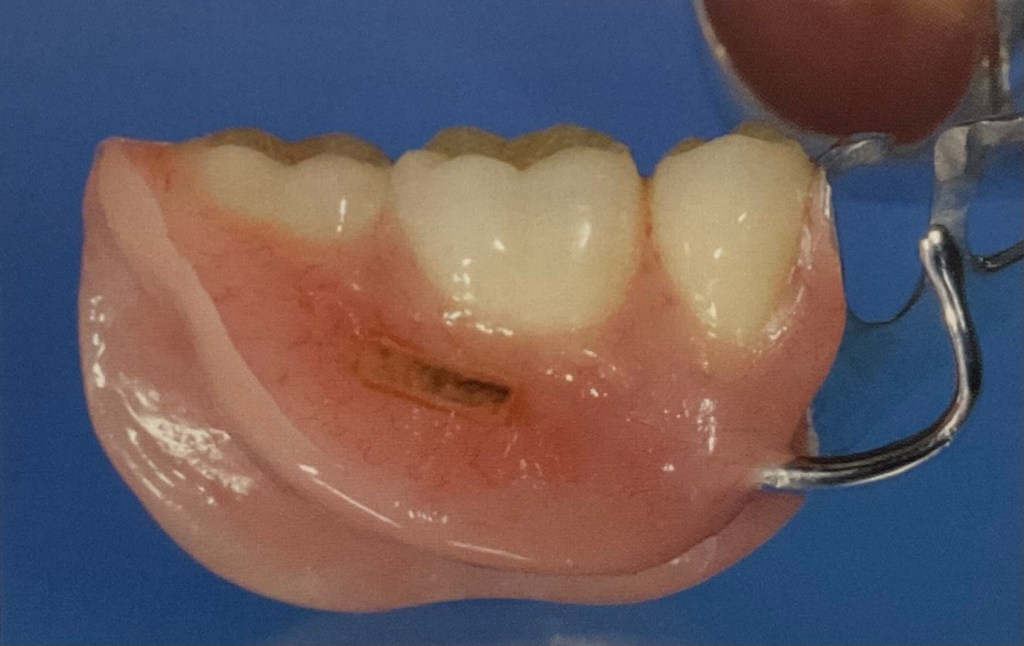
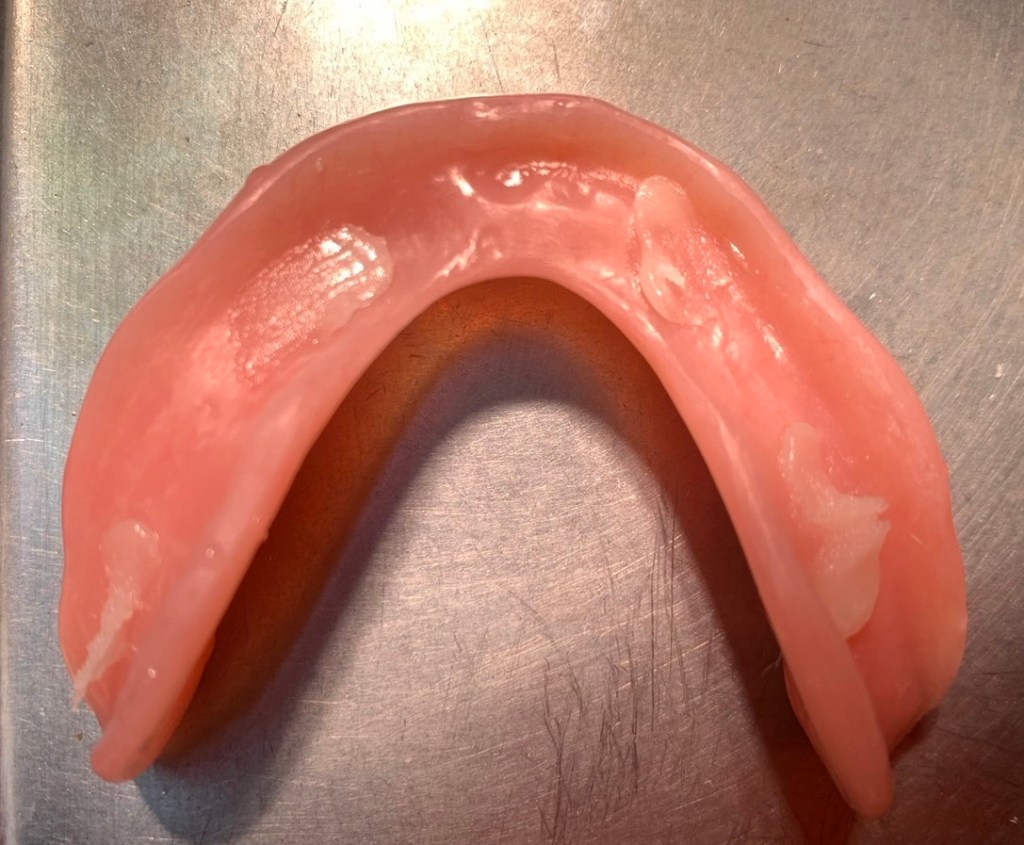
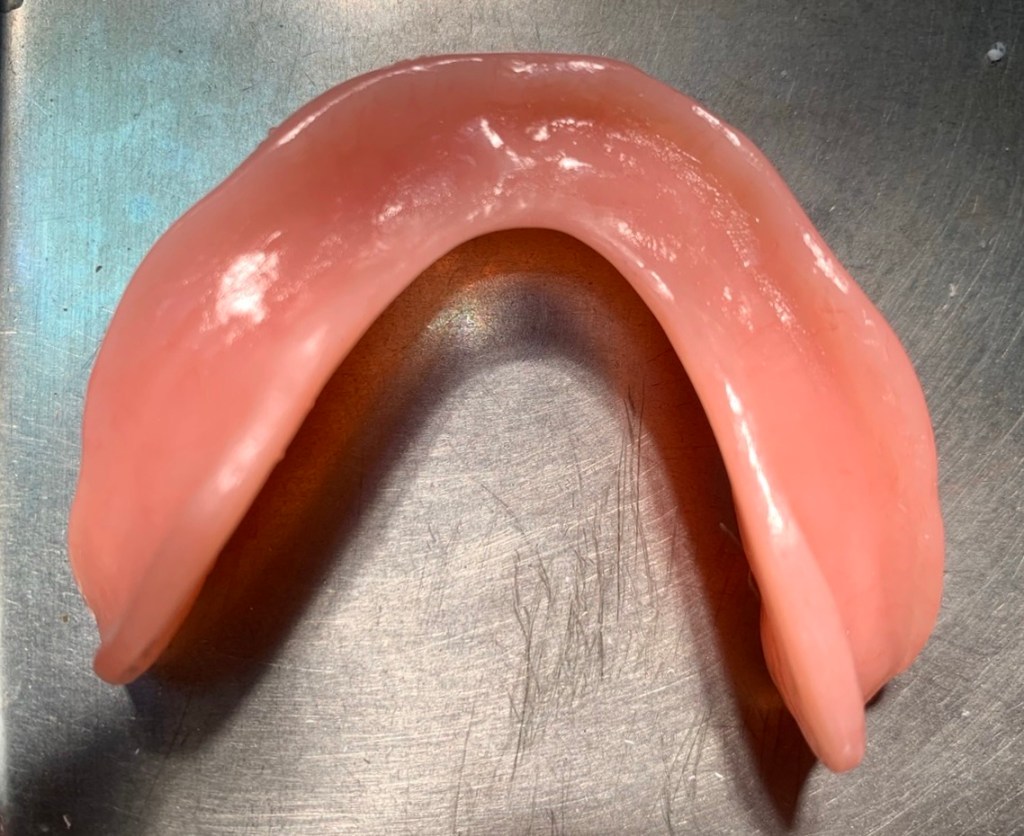
ตัวอย่าง ฟันปลอมชนิดที่มี อะคริลิค อย่างเดียว เป็นฟันปลอมชิ้นล่าง
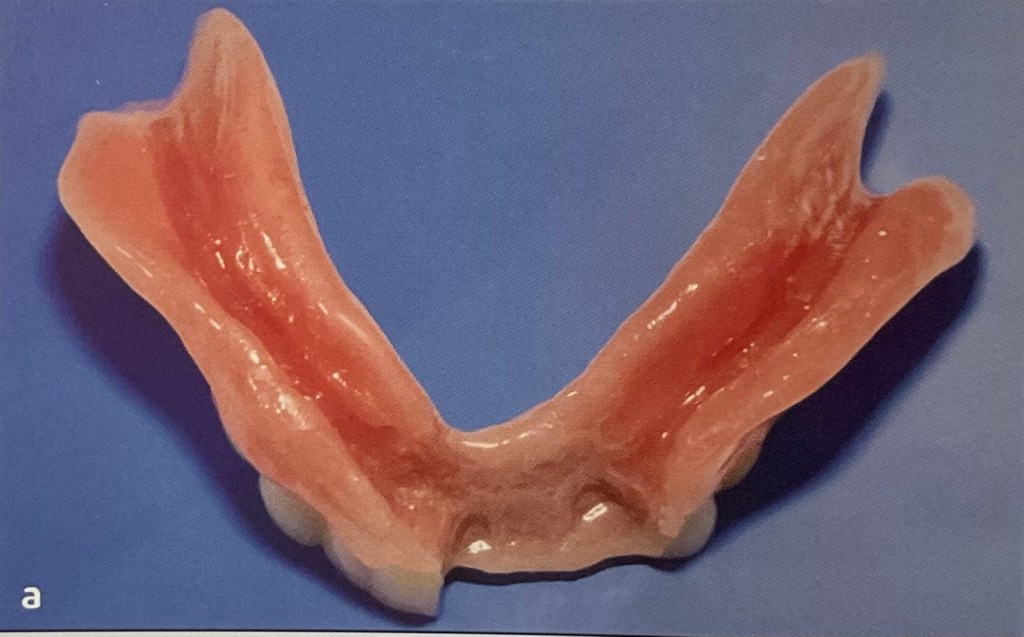
ฟันปลอมชิ้นเดียวกัน เมื่อดูด้านล่าง
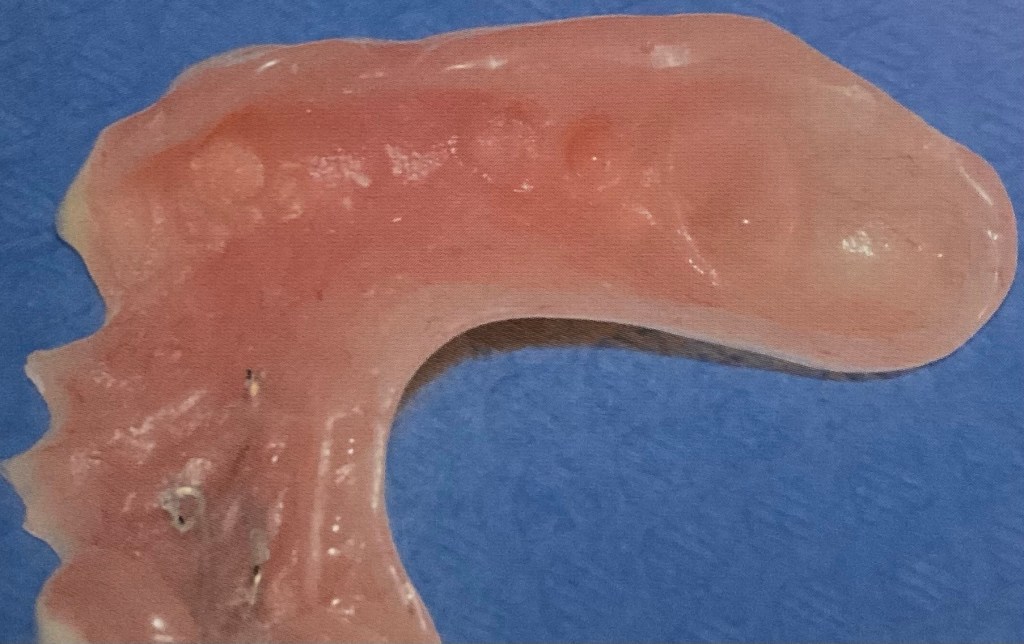
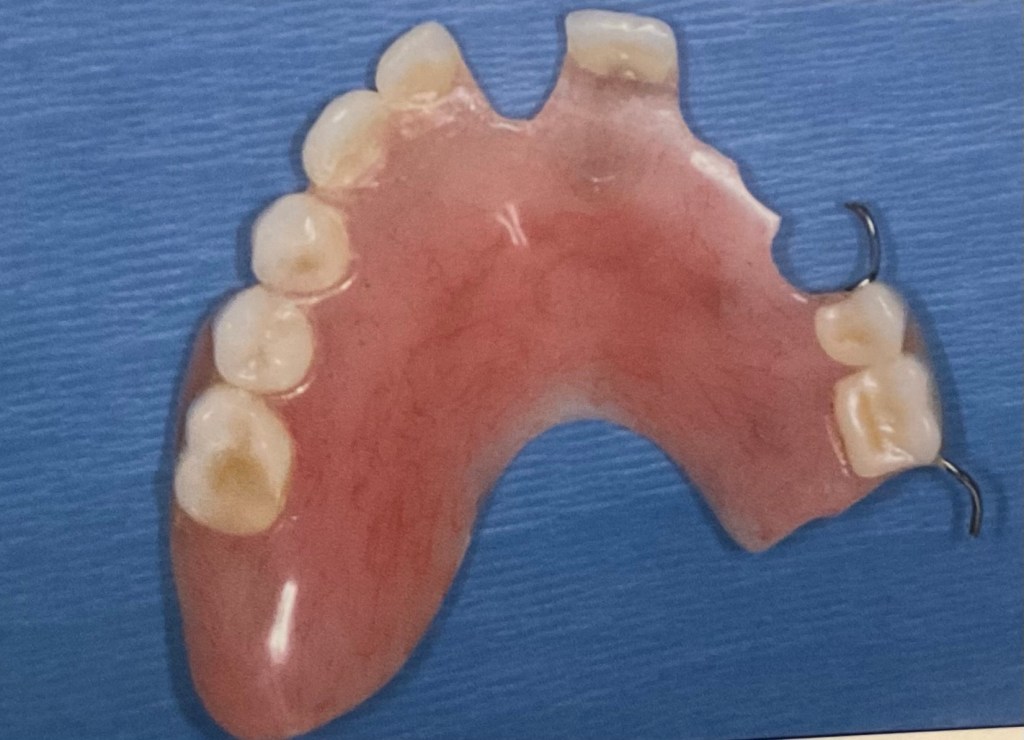
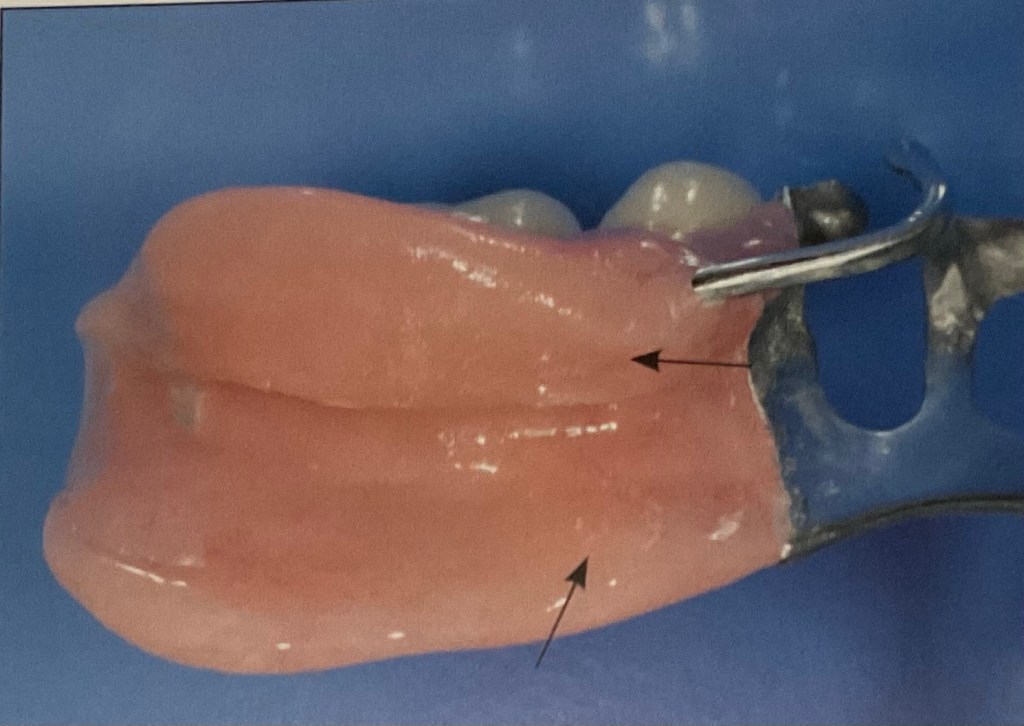
แสดงฟันปลอมชนิด ฐานอะคริลิค อีกชิ้น เป็นชิ้นฟันบน จะสังเกตว่า ด้านล่างฐานฟันปลอมจะมีลักษณะขรุขระ ผิวไม่เรียบ ซึ่งจำลอง ลอกเลียนรายละเอียดตามรูปร่างเหงือก และ เพดาน ของผู้สวมใส่แต่ละคน
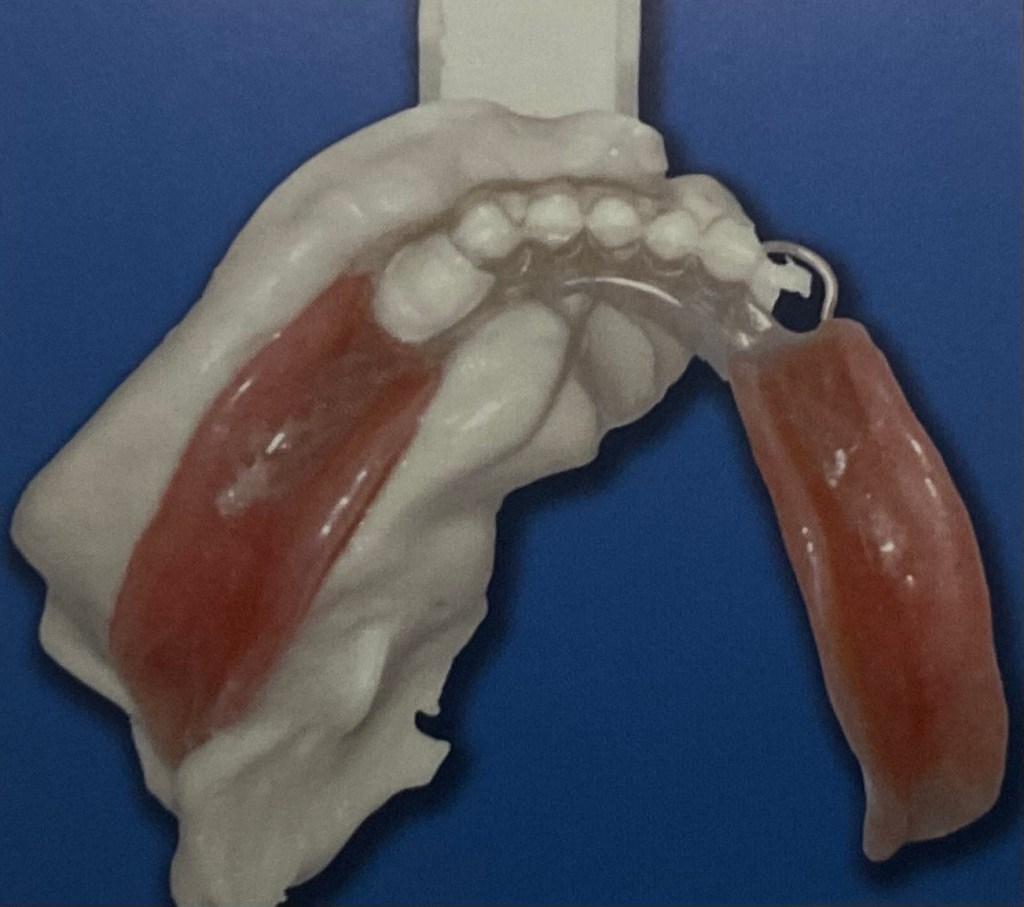
อีกชิ้น เป็นฟันปลอมชนิดที่ไม่มีโลหะ แต่เป็นฐานฟันปลอมแบบยืดหยุ่น คือ แข็งนะครับ ไม่นิ่ม เพียงแต่มันสามารถบิดงอได้ นิดหน่อย (ถ้าเป็นชนิด อะคริลิค แบบที่แสดงในตอนแรก จะบิดงอไม่ได้เลยครับ)
รูปนี้ สังเกตว่า ออกแรงบีบนิดหน่อย มันจะงอได้
การงอได้ของมัน มีไว้เพื่อให้สามารถโอบรัดที่ฟันจริง เป็นตัวที่ทำให้ฟันปลอมแน่น โดยไม่ต้องใช้ตะขอ ที่เป็นโลหะครับ
ฟันปลอมชนิดถอดได้ ที่ทำกันส่วนใหญ่ในประเทศไทย จะทำด้วย อะคริลิค ครับ
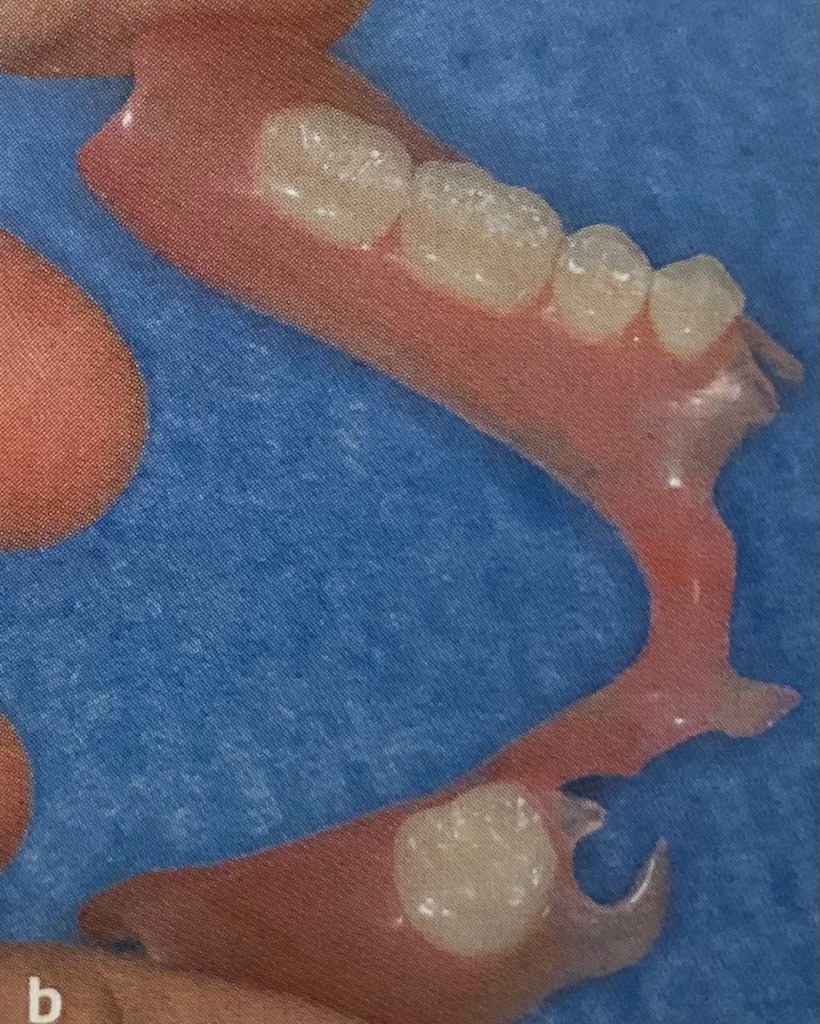
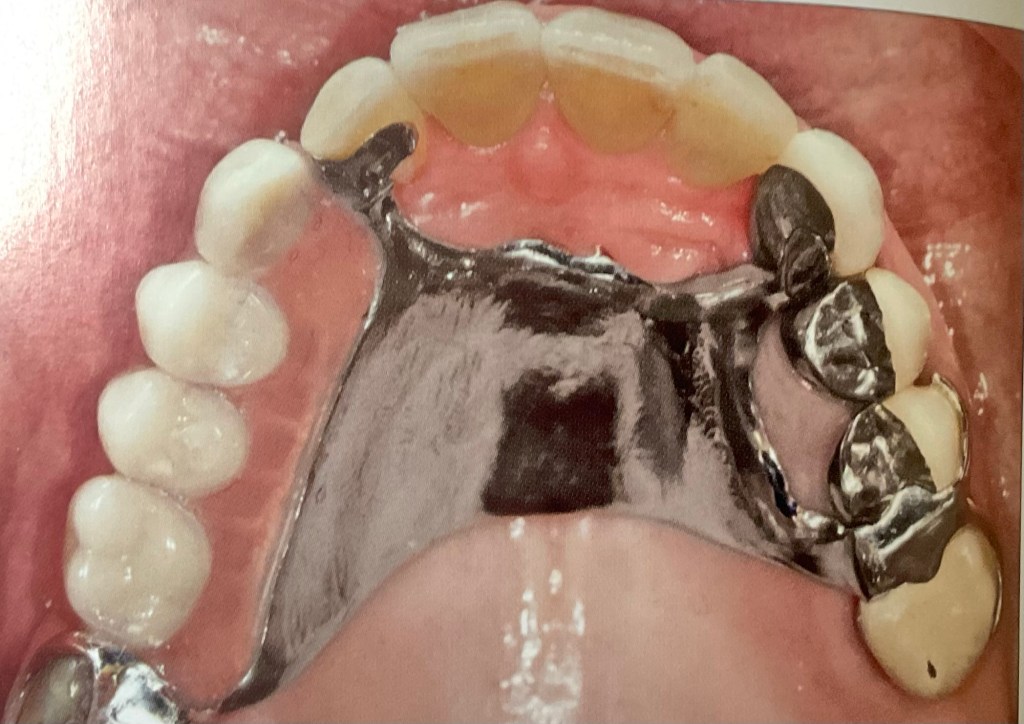
แบบนี้คือ แบบฐานอะคริลิค ที่มีตะขอโลหะอยู่ด้วย
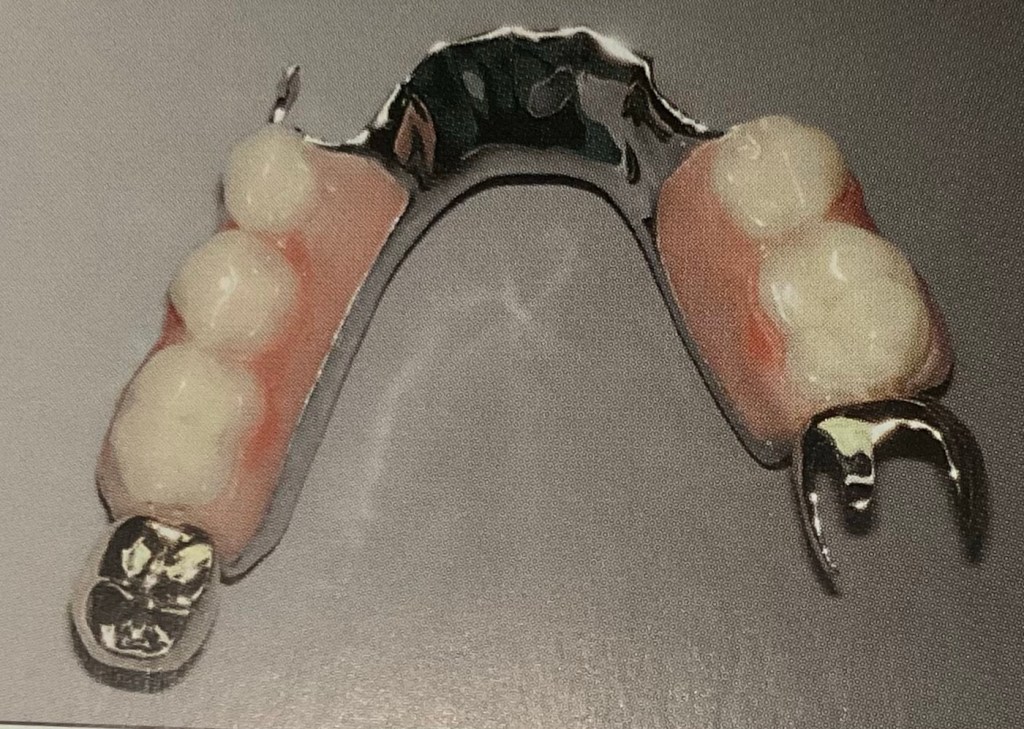
นี่ก็เป็น แบบ อะคริลิค กับ โลหะ เช่นกัน
โลหะที่ใช้เป็น โลหะผสมชนิด โคบอลต์+โครเมียม ไม่เกิดการกัดกร่อนในช่องปาก ไม่เกิดสนิม (แต่ไม่ใช้ Stainless steel นะครับ เราไม่ใช้ Stainless steel กับฟันปลอมครับ)
ในความความรู้สึกของ หมอที่ทำฟันปลอม การดูแลรักษาฟันปลอม นอกจากจะทำให้ฟันปลอมใช้ได้นานแล้ว ยังช่วยให้ฟันธรรมชาติ ที่เหลืออยู่ของผู้ใส่ มีอายุการใช้งานที่ยาวนานตามไปด้วย
เพราะฟันปลอม แม้ถือเป็นสิ่งประดิษฐ์ที่ไม่ได้ใช้งานเพื่อใส่ภายในร่างกาย เช่น โลหะผสมไทเทเนียม ที่ยึดดามกระดูก หรือ ลิ้นหัวใจที่ฝังอยู่ภายใน แต่ลักษณะการใส่ในช่องปาก ที่แนบสนิท และติดชิด กับอวัยวะโดยรอบ ทั้ง ฟัน, เหงือก, ลิ้น, กระพุ้งแก้ม, เพดานปาก ทำให้ถ้าทำความสะอาดฟันปลอมไม่ดี ย่อมมีผลต่ออวัยวะเหล่านี้ด้วย นี่ยังไม่นับ ขณะฟันปลอมทำงานเคี้ยวอาหาร ก่อนอาหารถูกกลืนผ่านลงไป
รูปแสดงการวางในตำแหน่งของฟันปลอมบน
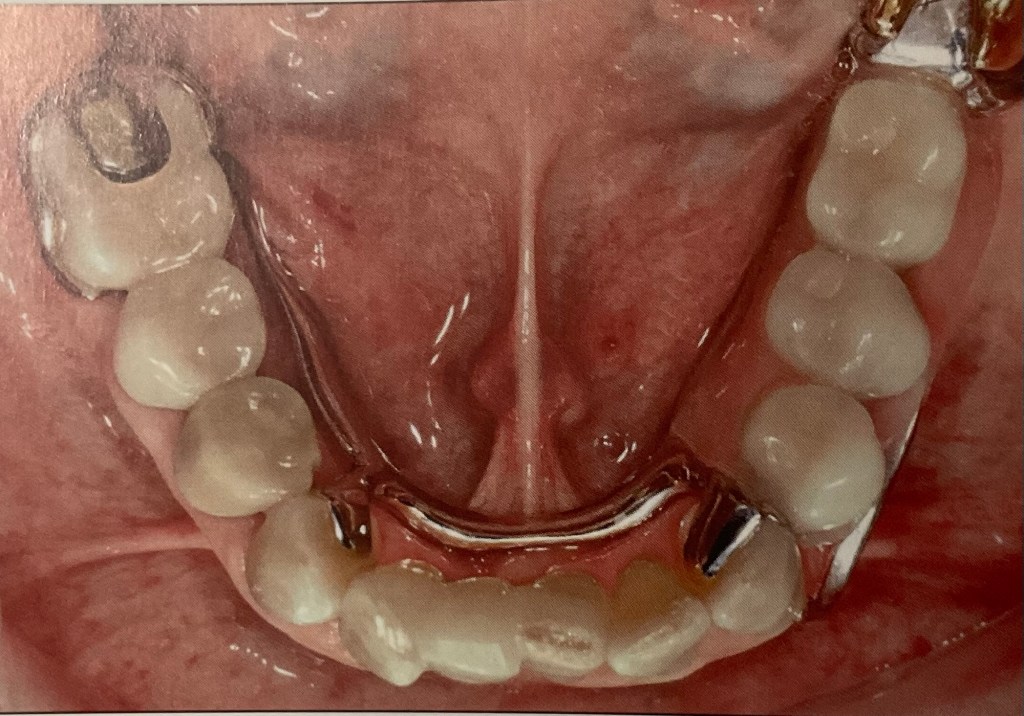
ขณะวางอยู่ในตำแหน่งของฟันปลอมล่าง
จึงจะเห็นว่า การทำความสะอาดและดูแลฟันปลอม สำหรับผู้สูงอายุจึงเป็นสิ่งสำคัญมาก เพราะถ้าทำความสะอาดได้ไม่ดี อย่างน้อยที่สุด ผลเสียจะตกกับอวัยวะที่เกี่ยวข้องกับมันมากที่สุด คือ เกิดฟันผุ และ โรคเหงือกอักเสบ นั่นเอง
หลักในการดูแลฟันปลอม แบบพื้นฐาน
ทำความสะอาดฟันปลอม ทุกครั้ง หลังมื้ออาหาร
รูปแสดง แปรงทำความสะอาดฟันปลอมโดยเฉพาะ ที่มีหัวแปรง 2 แบบ หัวที่กว้างใช้แปรงผิวทั่วไป ส่วนหัวเล็กใช้แปรงบริเวณซอกเล็กๆ
เราดัดแปลงการใช้งาน โดยมีแปรง 2 ขนาดได้ครับ แปรงหัวใหญ่ปกติ กับ แปรงขนาดหัวเล็ก เช่น แปรงเด็ก เวลาใช้งาน ก็ใช้ทำความสะอาดด้วยกัน
ยกตัวอย่าง ส่วนของฟันปลอมที่เป็นซอกเล็กๆ นะครับ แปรงขนาดหัวปกติจะเข้าไปทำความสะอาดตรงนี้ยาก
คือ บริเวณด้านในตะขอโลหะ
2. สารที่ใช้ทำความสะอาดฟันปลอม ร่วมกับแปรงสีฟัน ได้ดีที่สุด คือ น้ำยาล้างจานครับ และ ตัวทำความสะอาดที่แย่ที่สุด คือ ยาสีฟัน
เหตุผล คือ ตัวฐานฟันปลอม และ ซี่ฟันปลอม จะสึกได้เมื่อเจอผงขัดที่อยู่ในยาสีฟันครับ ขณะที่น้ำยาล้างจาน ไม่มีผงขัดผสม จึงเป็นตัวที่ปลอดภัยที่สุด ไม่ทำให้ฟันปลอมเกิดรอยขีดข่วน หรือ ฟันปลอมสึกในระยะยาว
ในความเห็นส่วนตัว ของหมอทำฟันปลอม ไม่ serious ครับ ถ้าท่านใดชอบการใช้ยาสีฟัน ก็ใช้ได้เลย
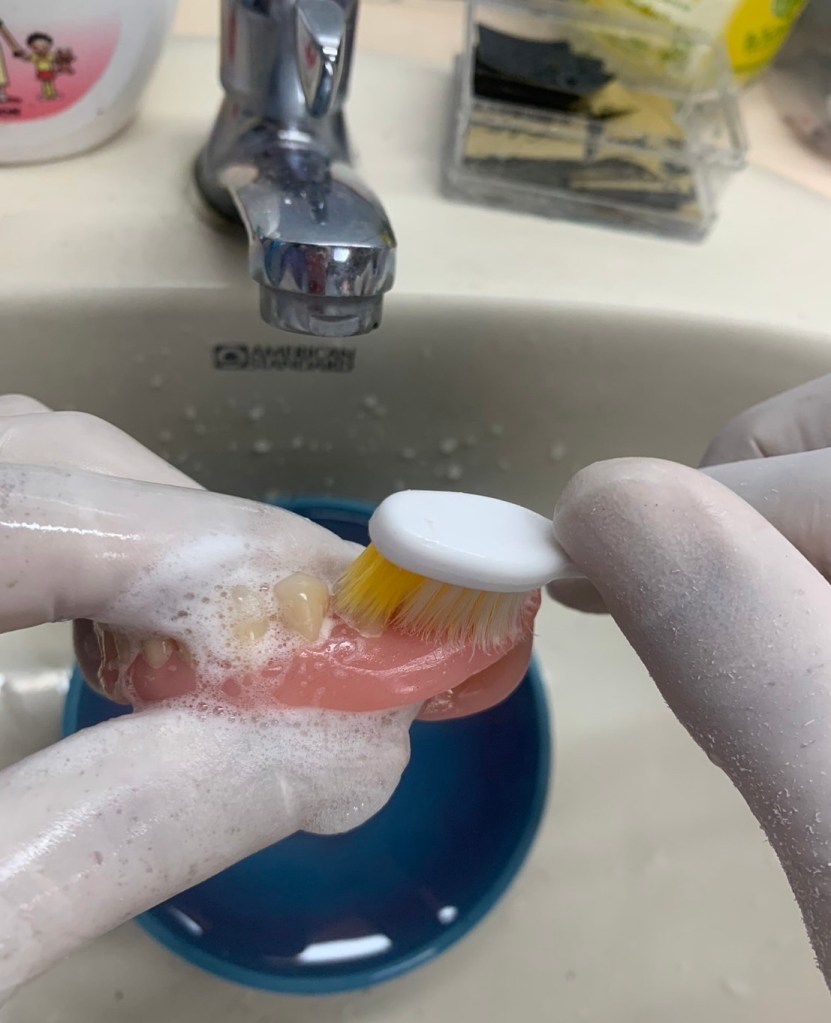
3. ขณะแปรงฟันปลอม ควรทำที่อ่างน้ำ และ เปิดน้ำในอ่างคาไว้เล็กน้อย อย่าทิ้งน้ำหมด คือ เผื่อพลาด เกิดฟันปลอมหลุดมือครับ น้ำในอ่างจะช่วยพยุงฟันปลอมที่พลัดหล่นได้ ไม่เกิดความเสียหาย
ถ้าท่านใด ไม่สะดวกทำใกล้อ่างน้ำ ให้ใช้ขันน้ำใส่น้ำ รองไว้ใกล้ๆ มือครับ
4. ต่อเนื่องจากข้อ 3 คือ สมมติพลาด เกิดสถานการณ์ที่ฟันปลอมหลุดมือ หล่น แล้วร้าว หรือ หักออกเป็นชิ้นๆ ถ้าเก็บชิ้นส่วนมาครบ ส่วนใหญ่ 90% จะต่อกลับคืนได้ครับ ไม่ต้องทำชิ้นใหม่
เก็บชิ้นส่วนให้ครบ ไม่ต้องพยายามทากาวยึดเชื่อมกลับครับ เพียงเก็บครบ แล้วส่งมาถึงมือหมอเท่านั้น ในหลายกรณี คนใส่ไม่จำเป็นต้องไปด้วย เมื่อซ่อมเสร็จ ให้คนอื่นในบ้านมารับฟันปลอมนำให้กลับไปใช้ได้ กรณีผู้สูงอายุติดเตียงครับ
ยกเว้น ในบางกรณี ถ้าหมอตรวจฟันปลอมดูแล้ว ไม่สามารถซ่อมโดยไม่มีผู้ใส่ได้ ก็จำเป็นต้องให้เจ้าของฟันปลอมมาด้วย เพื่อพิมพ์แบบซ่อมฟันปลอมครับ
รูปแสดงการพิมพ์แบบเพื่อซ่อมฟันปลอม ที่ต้องพาเจ้าของฟันปลอมมาด้วย เพื่อพิมพ์
5. ปกติการเก็บฟันปลอม เมื่อถอดออกตอนนอนกลางคืน ควรแช่ฟันปลอมในน้ำครับ
ใช้น้ำสะอาดธรรมดา ไม่จำเป็นต้องแช่ในน้ำยาฆ่าเชื้อทุกคืน
เหตุผล คือ เป็นการรักษาฟันปลอมให้อยู่ในสภาพที่ชื้นเหมือนเวลาใส่ในปากตลอดเวลาครับ ฟันปลอมสามารถเก็บไว้ในที่แห้งได้ แต่ถ้าแห้งเป็นระยะเวลานาน ส่วนของฟันปลอมที่เป็นฐานอะคริลิค อาจเกิดการเปลี่ยนรูปร่างได้ เมื่อเทียบกับตอนที่มันอยู่กับน้ำลาย
6. เทคนิคการทาครีมติดฟันปลอม
ขั้นตอนแรก บีบจากหลอดออกมาไว้ที่ใต้ฐานฟันปลอม เป็นจุดๆ ครับ 2-3 จุด
จากนั้นใช้นิ้วเกลี่ยให้ทั่ว เป็นชั้นบางๆ เหมือนเราทาครีมที่ใบหน้า
เป็นชั้นบางๆ แบบนี้ (ไม่เหลือให้เห็นเป็นก้อน หรือ ชั้นหนา)
เหตุผล เพราะ เมื่อครีมติดฟันปลอม ถูกน้ำลายจะเกิดการดูดน้ำ แล้วขยายตัว หรือ พองตัวแบบช้าๆ ทำให้เกิด “ความหนืด” เพิ่มขึ้นครับ การทาเป็นชั้นบางๆ ทำให้ฟันปลอมสามารถแนบสนิท ใส่ลงตำแหน่งได้ ถ้าทาเป็นก้อน หรือ ชั้นหนา โดยไม่เกลี่ยให้เสมอกัน ครีมส่วนเกินจะไหลออกจากฐานฟันปลอม เกิดการละลายได้เร็ว
ละลายได้เร็วจาก ครีมเมื่อดูดน้ำจนหนืดสูงสุดแล้ว ถ้ามีน้ำให้ดูดเข้าไปอีก ความหนืดของมันจะลดลงอย่างรวดเร็ว แล้วเกิดการละลายครับ ทำให้คนที่ใช้รู้สึก ต้องทาครีมยึดบ่อยกว่าที่ควรจะเป็น
ต่อไป เป็นช่วงคำถามครับ
ref:
https://thaipublica.org/2024/02/thailand-becomes-aged-society/#:~:text=สังคมผู้สูงอายุโดยสมบูรณ์,ละ%2014%20ของประชากรทั้งหมด https://3doctor.hss.moph.go.th/main/rp_ampur?rgion=5&prov=NzM=&provn=4LiZ4LiE4Lij4Lib4LiQ4Lih https://ppdental.anamai.moph.go.th/elderly/2553/EldGr/HPPEld3.pdf https://www.quintessence-publishing.com/gbr/en/product/noncarious-cervical-lesions-and-cervical-dentin-hypersensitivity https://www.quintessence-publishing.com/gbr/en/product/brudviks-advanced-removable-partial-dentures https://ppdental.anamai.moph.go.th/elderly/academic/full91.pdf
โดย เรืออากาศเอก ทันตแพทย์ พัลลภ ตรีนัย ท.บ.
-ทันตแพทยศาสตร์บัณทิต (เกียรตินิยม อันดับ 1) คณะทันตแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่ (พ.ศ. 2532-2537)
-หลักสูตรวิทยาศาสตร์มหาบัณฑิต ภาควิชาทันตกรรมประดิษฐ์ คณะทันตแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย (พ.ศ. 2541-2543)
-แผนกทันตกรรม โรงพยาบาลภูมิพลอดุลยเดช กรมแพทย์ทหารอากาศ กองทัพอากาศ (พ.ศ. 2544)
-คลินิกอารักษ์ทันตแพทย์ (พ.ศ.2544 – ปัจจุบัน)
สถานที่ติดต่อ : 100-102 คลินิกอารักษทันตแพทย์ ถ.พญาพาน ต.พระปฐมเจดีย์ อ.เมือง จ.นครปฐม 73000 (034-259 117)