Pharmacodynamic ของยาชาที่คุ้นเคยในรูปนี้
ครั้งแรกเมื่อมองผ่านๆ ผมเข้าใจว่า น่าจะเป็น Lidocaine ที่พวกเราคุ้นเคยที่สุด แต่พบว่า มันไม่ใช่ครับ
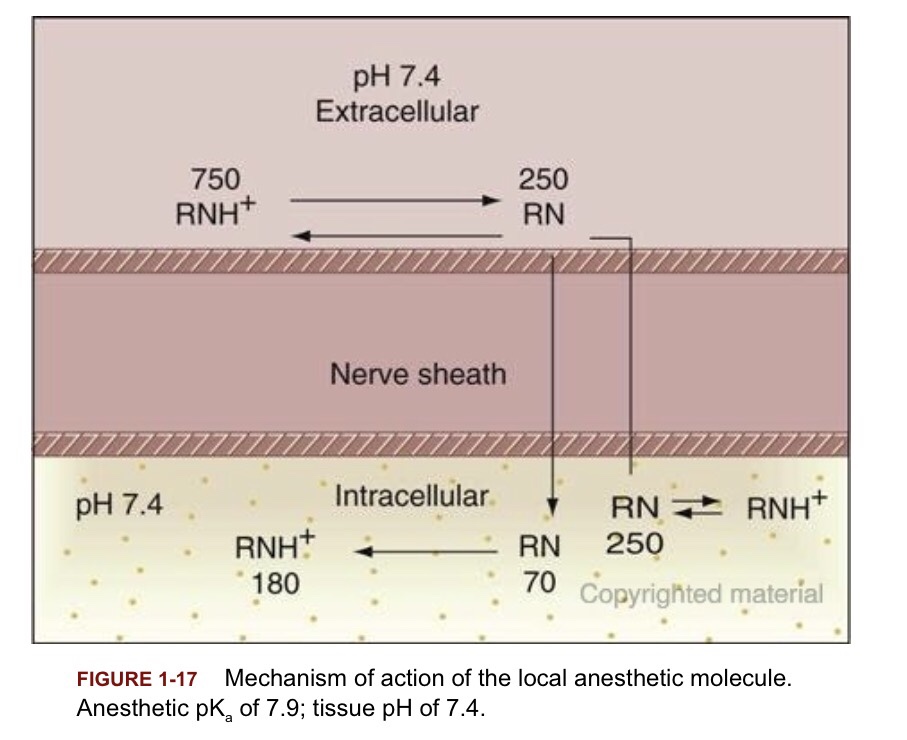
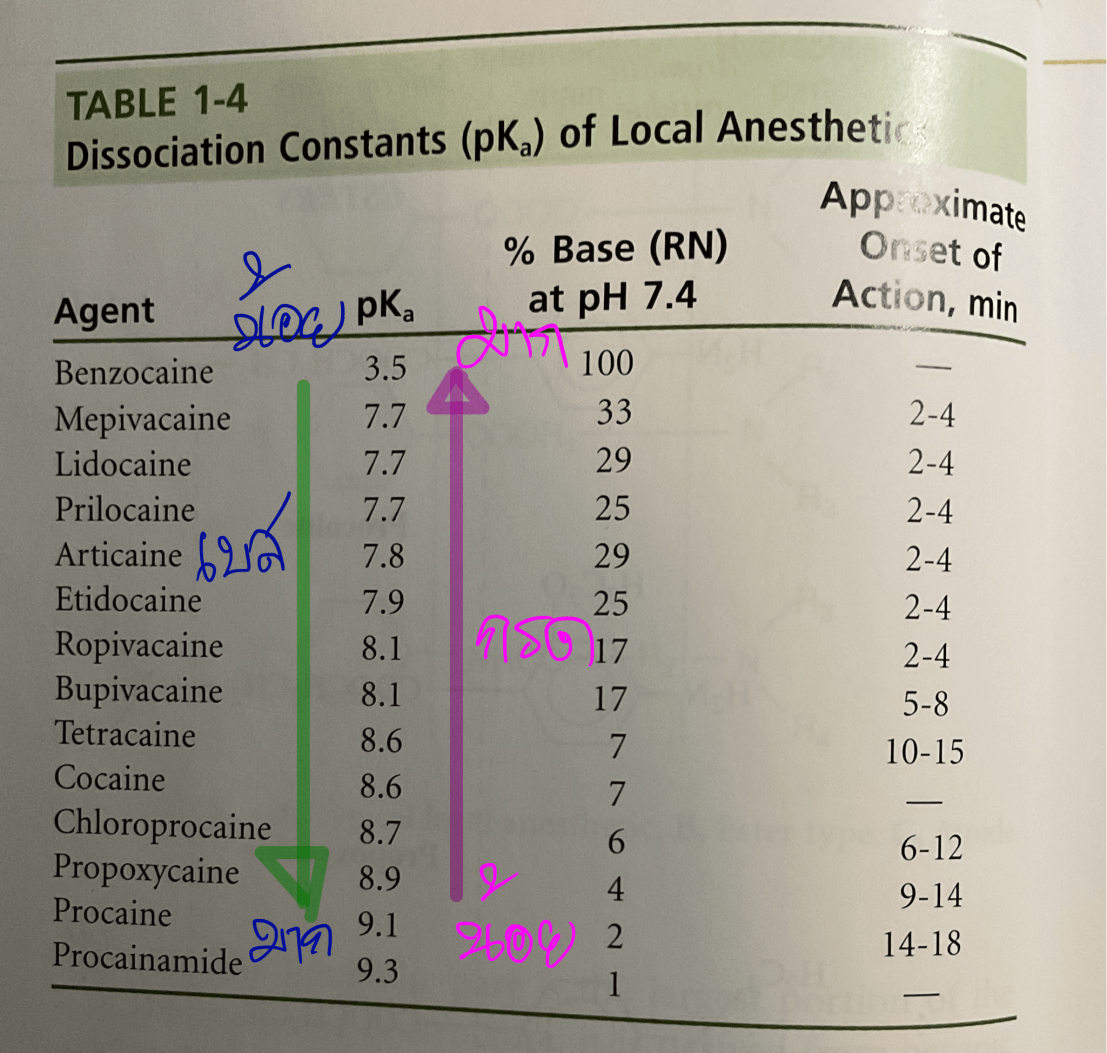
ถ้าดูตามตารางแล้ว pKa = 7.9 ตัวนี้คือ Etidocaine (เข้าใจว่าที่ใช้ตัวนี้เป็น model เพราะคิดตามสมการแล้วจะได้ การปัดเป็นจำนวนที่ลงตัว และสื่อความหมายได้ง่ายที่สุด)
ให้มองที่ column % Base (RN) at pH 7.4
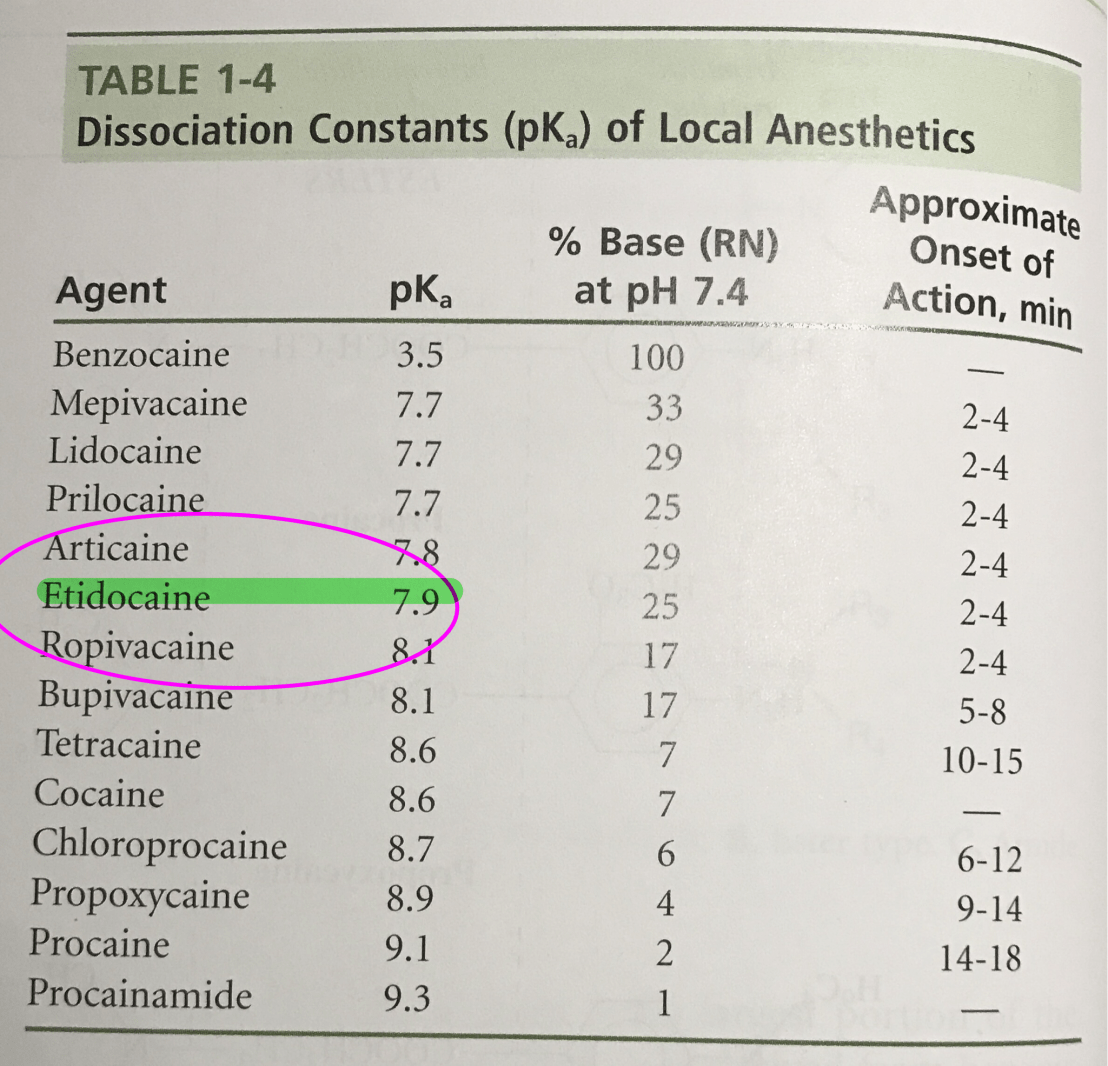
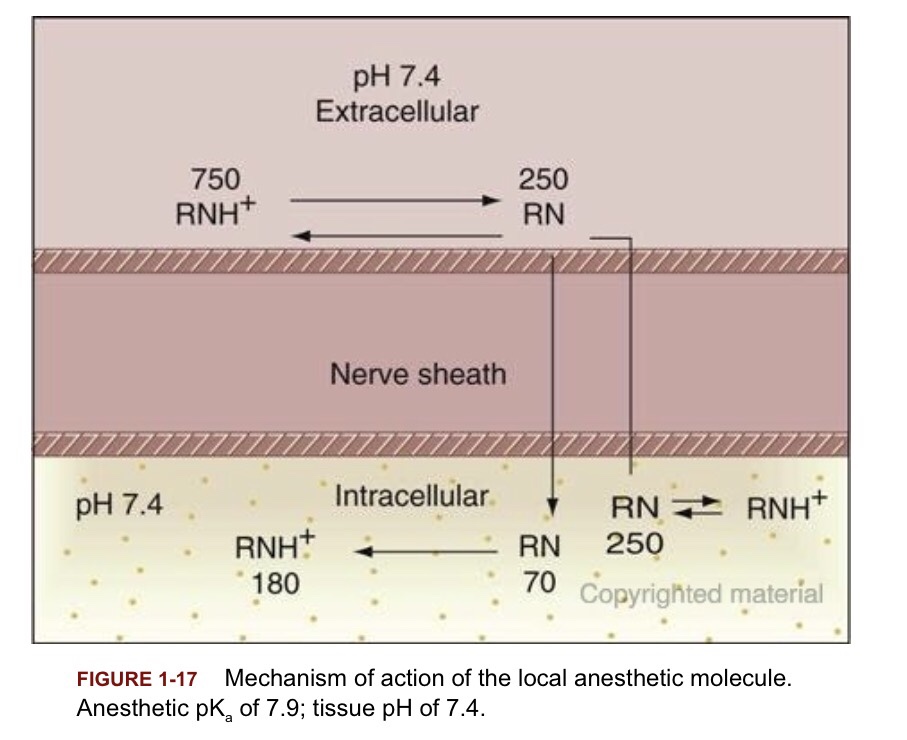
แล้วกลับมามองที่รูปนี้อีกครั้ง
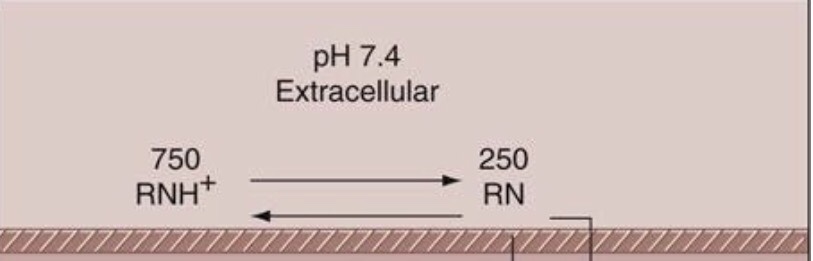
ในการสมมติที่โมเลกุล Etidocaine 1,000 โมเลกุล จาก table 1-4 แตกตัวให้ [RN] 25%
จากรูป จึงเป็น [RNH+] 750 โมเลกุล + [RN] 250 โมเลกุล = 1,000 โมเลกุล
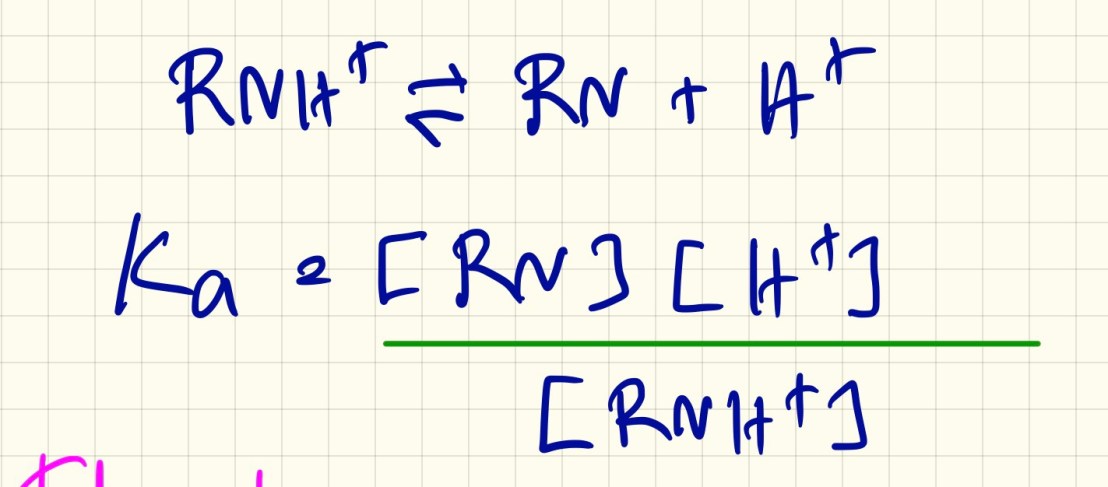
แสดงที่มาด้วย Henderson-Hasselbalch equation ได้ดังนี้
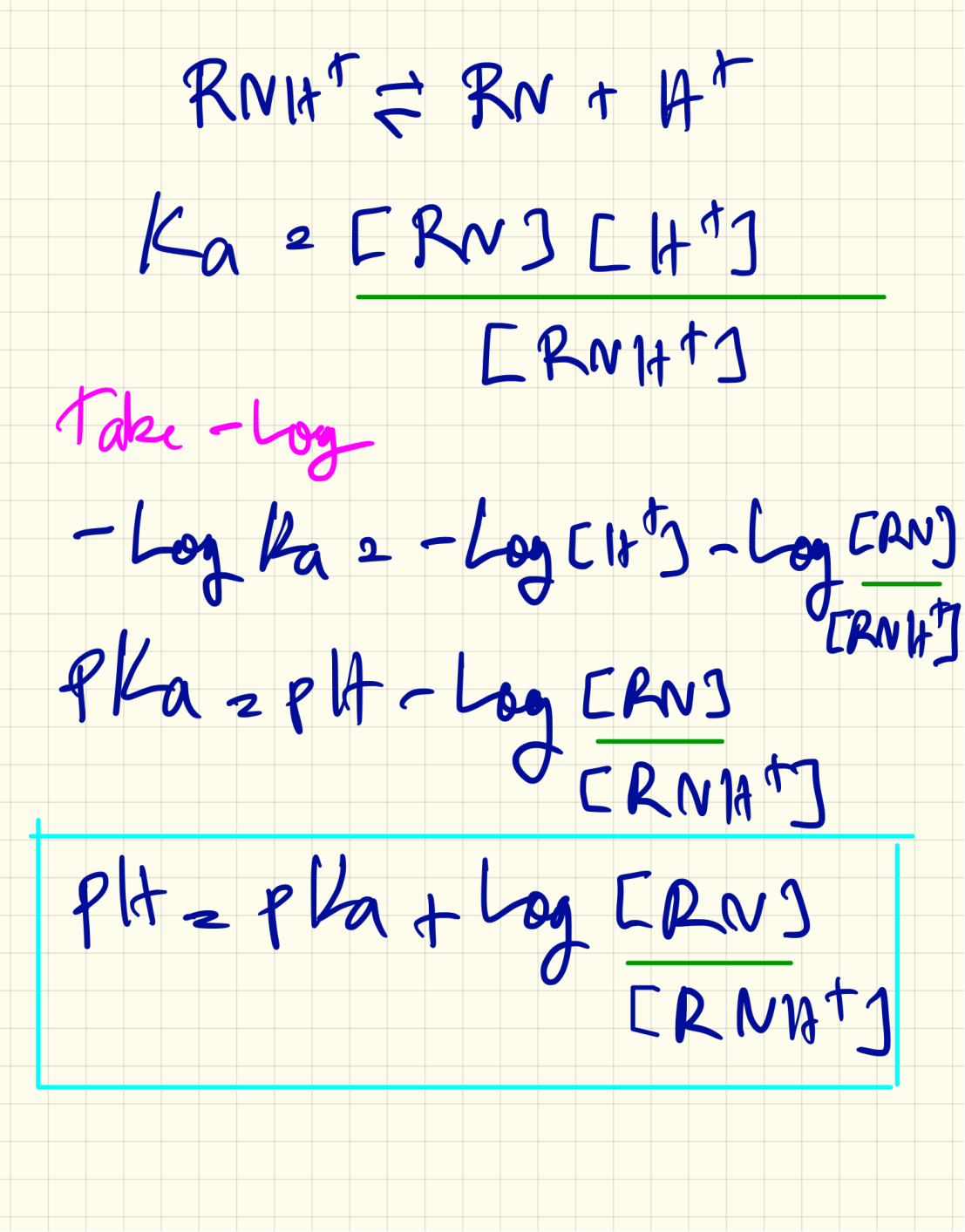
ความสัมพันธ์ของ Ka คิดขึ้นมาโดย Lawrence Joseph Henderson จากการศึกษาเรื่อง Blood gas analysis ในปี ค.ศ. 1908 (พ.ศ. 2451 ก่อนปีสวรรคตของ ร.5 เพียง 2 ปี)
ส่วนประกอบนี้ Henderson เป็นผู้คิด
Lawrence Joseph Henderson

แต่ในปีนั้น โลกยังไม่รู้จักคำว่า pH ครับ
ต้องรออีก 1 ปี คือ ปี ค.ศ. 1909 Søren Peter Lauritz Sørensen เป็นผู้ให้กำเนิด definition ของ pH

ทำให้ในปีเดียวกัน Karl Albert Hasselbalch เป็นผู้ทำให้สมการชุดนี้สมบูรณ์ ด้วยการ take Log เข้าไป
Hasselbalch take Log สมการทั้งหมด (เมื่อรวมกับ pH ที่ Sorensen นิยามไว้ สมการจึงสมบูรณ์)

Karl Albert Hasselbalch

ต่อไปนี้จะเป็นการพิสูจน์ตัวเลขใน Textbook ” Handbook of LOCAL ANESTHESIA” ของ Stanley F. Malamed ในบทที่ 1 ด้วยสมการ Handerson-Hassalbalch นะครับ ถ้าใครที่ไม่สนใจเรื่องตัวเลขว่ามีที่มายังไง? ให้ผ่านส่วนนี้ของบทความไปเลยครับ (ผมจะจบ part นี้ด้วยคำว่า “สิ้นสุดการพิสูจน์”)
ลองทดสอบ สมการนี้ในการอธิบายตัวเลขชุดแรกในรูป
ข้อมูลที่มีคือ tissue มี pH = 7.4 และ Etidocaine มี pKa = 7.9

แก้ Log


นั่นคือ Etidocaine 1,000 โมเลกุล จะแตกตัวให้
[RN] = 24% = 240 โมเลกุล
[RNH+] = 76% = 760 โมเลกุล
หลังจากนั้น [RN] ~ 250 โมเลกุล diffuse ผ่าน nerve sheath
จึงมีการปรับสมดุลใหม่ของ [RNH+] ที่มีอยู่เดิม ~ 750 โมเลกุล ใหม่ เป็นการแตกตัวรอบ 2

[RN] = 180 โมเลกุลที่ถูกสร้างรอบที่ 2 ก็จะ diffuse เข้าไปใน nerve sheath รอบใหม่ตามรูป
ในรอบนี้ สมดุล [RNH+] จะ = 569.82 ~ 570 โมเลกุล

จากนั้น ขบวนการเกิด Reequilibration อีกครั้ง (รอบที่ 3,4,…จนสารตั้งต้นหมด) ในสมการซ้ำเดิมที่
[RN]/[RNH+] = 0.3162
แต่จำนวนโมเลกุลของ Etidocaine ตั้งต้นที่เปลี่ยนไปในแต่ละรอบ
เช่น [RNH+] 180 โมเลกุล + [RN] 70 โมเลกุล = โมเลกุลทั้งหมด 250 (ในรอบใหม่) เสมอ ตามรูป
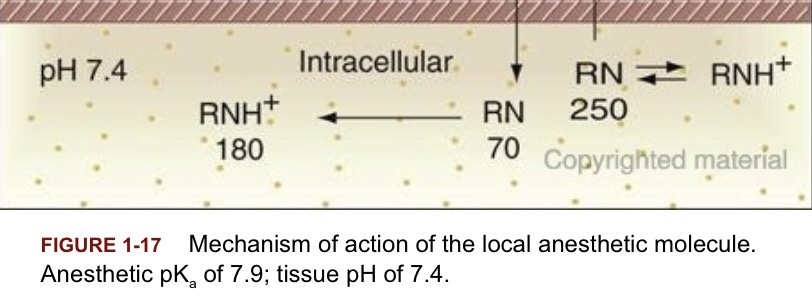
ในรูปด้านล่างก็ใช้หลักการเดียวกัน แต่อย่าลืมว่า
สำหรับ Etidocaine ในเงื่อนไข
[RN}/[RNH+] = 0.3162 หรือ ratio [RN] + [RNH+] = 25 %+ 75 %= 100 % ต้องเกิดในสภาวะที่ tissue มี pH = 7.4 เท่านั้น
ถ้า pH ของสภาวะแวดล้อมเปลี่ยนไป เช่น pH = 6 ค่า Ka ของ Etidocaine (หรือยาชาใดๆ) จะไม่ได้อยู่ที่ค่าเดิม แบบใน table 1-4 นะครับ
แต่เมื่อ RN diffuse ผ่าน nerve sheath ได้แล้ว เมื่อไปเจอสภาวะ pH = 7.4 ก็คิดการแตกตัวตามหลักเดิมได้
ยกตัวอย่างในรูป เมื่อ [RN] ผ่านเข้าไป 10 โมเลกุลแล้ว ก็จะเข้าสู่สมดุลใหม่ (ratio 0.3162)
ได้ [RN] + [RNH+] = 25% + 75% = 2.5 โมเลกุล + 7.5 โมเลกุล = 10 โมเลกุล ดังแสดงในรูป
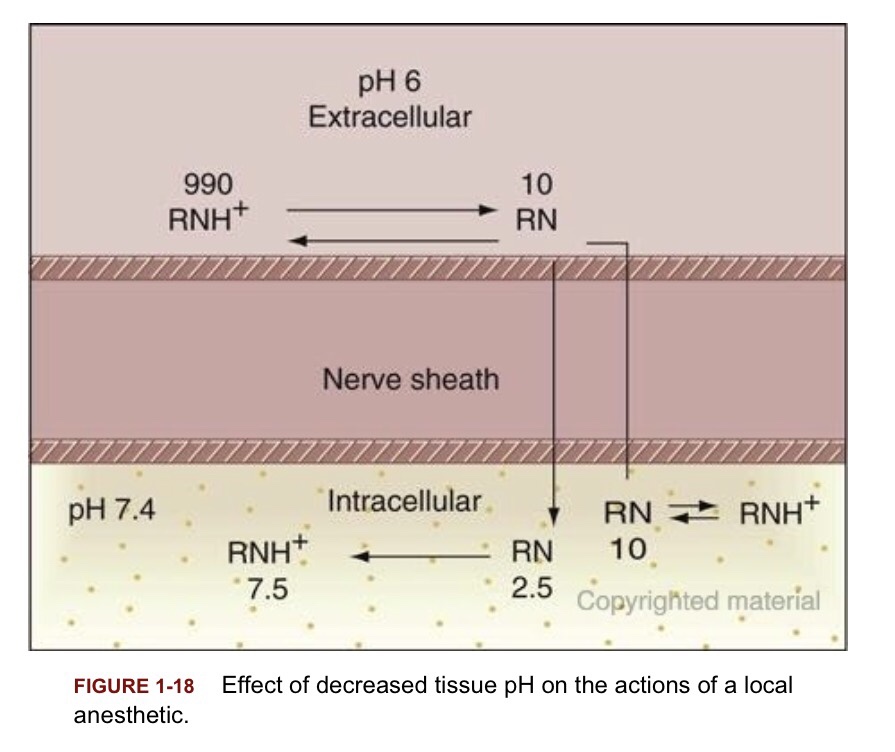
“สิ้นสุดการพิสูจน์”
สมการนี้ ไม่มีความจำเป็นต้องจำด้วยการท่องจำ เราสามารถทำความเข้าใจ และนำไปใช้ในทางคลินิกได้ ด้วยวิธีต่อไปนี้
ให้ลองดูสมการเคมีเดิม

สมการจะตั้งต้นด้วย RNH+ เพราะยาชา ในที่นี้ขอยกตัวอย่างจริงไปเลยละกัน คือ Articaine
Articaine จะอยู่ในรูปเกลือ โดยทำให้อยู่ในรูปสารละลาย Articaine HCl
(รสขมของยาชาที่ Pt รู้สึกเวลายาชา leak คือ รสชาติของ HCl salt ไม่ใช่จาก Articaine)
เมื่อยาชาเข้าไปอยู่ใน Extracellular fluid ยาชา Articaine HCl จะเกิดการละลายเปลี่ยนจาก salt กลายเป็น Articaine ที่ติดประจุ +
Articaine ใน Extracellular fluid คือ Articaine+ —> RNH+
จากนั้น Articaine+ <–> Articaine (ที่สูญเสีย Proton) + (H+)
ตามสมการ RNH+ <–> RN + (H+)

(ปริมาณยาชา = % x ปริมาตร x 10 = 4 x 1.7 x 10 = 68 mg/cartridge
ปริมาณ epinephrine = ปริมาตร x 10 = 1.7 x 10 = 17 μg/cartridge , 1:100,000 (ถ้า 1:200,000–> เอา 2 หาร = 8.5 μg, ถ้า 1:50,000 –> เอา 2 คูณ = 34 μg)
max dose = 7.0 mg/kg หรือ 440 mg
Epinephrine = 200 μg/visit, ใน Pt CVS = 40 μg/visit)
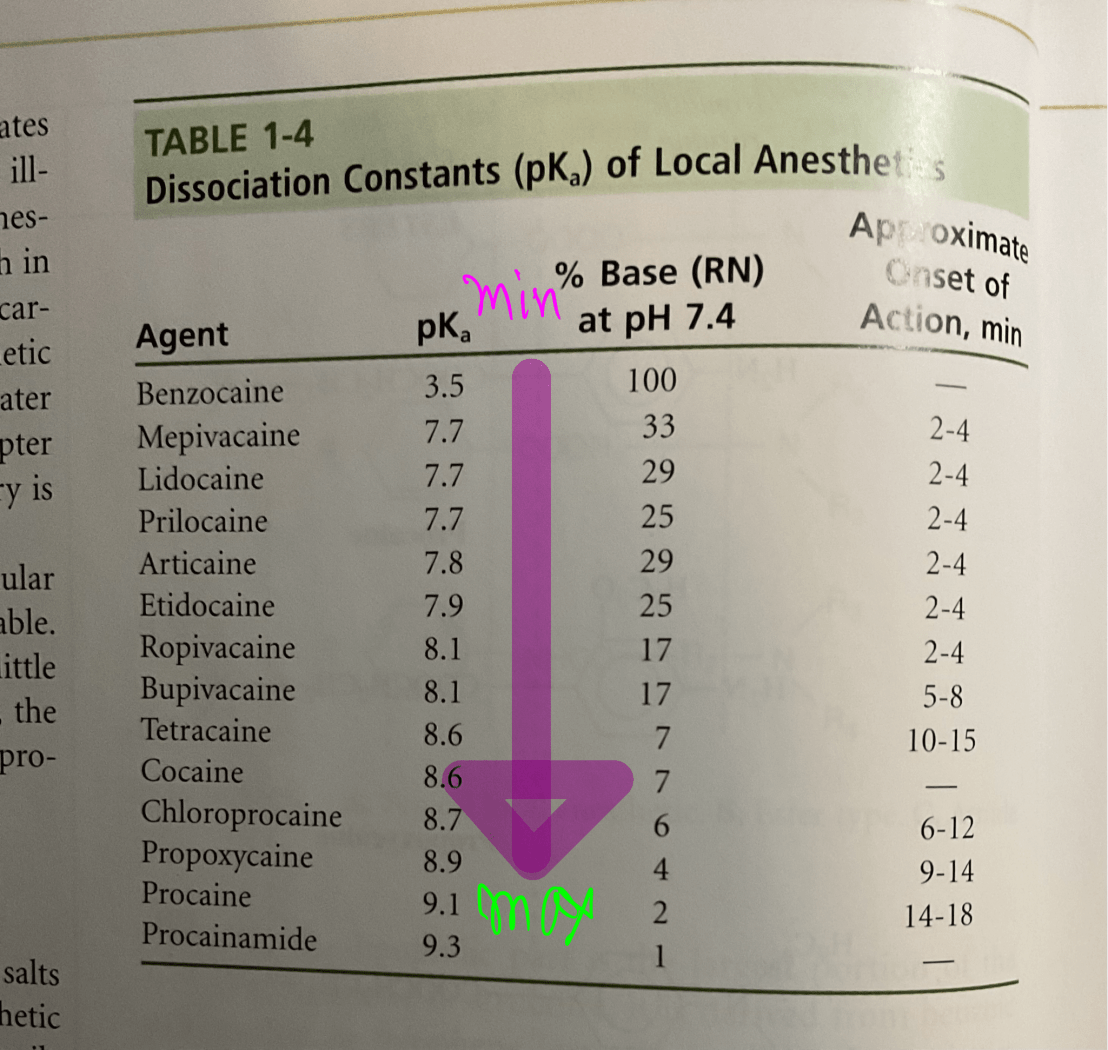
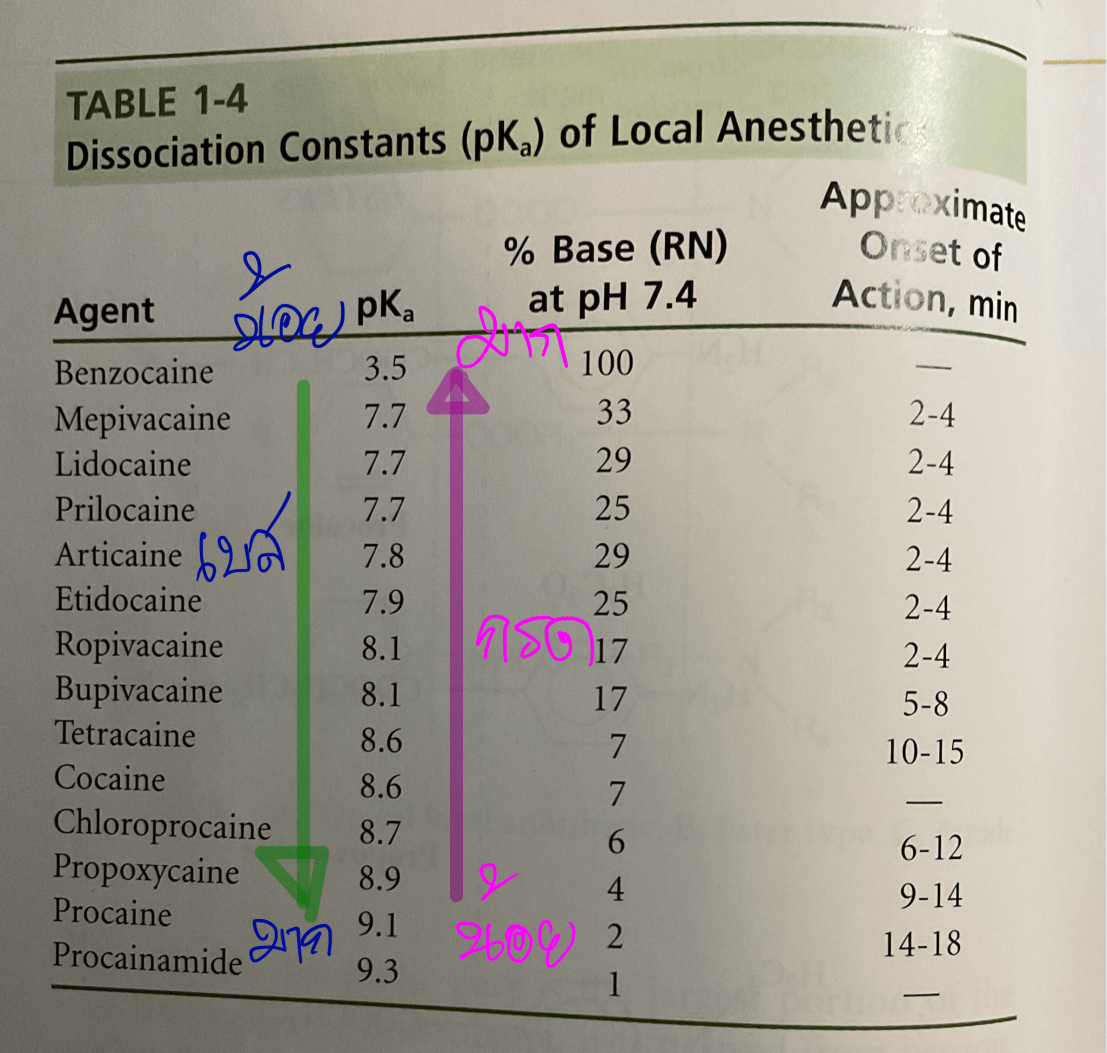
ทีนี้ถ้าเรามองย้อนกลับมาที่ ตารางนี้ซ้ำอีกครั้ง จะเห็นว่า ค่า pKa ของยาชาใน column แรก จะถูกเรียงจาก น้อยสุด —> มากสุด
คือ pKa ของ Benzocaine < Mepi, Lido, Prilo < Articaine < Etido < Ropi, Bupi < Tetra, Cocaine < Chloro < Propoxy < Procaine และ Procainamide มีค่า pKa มากที่สุด
จากสมการ Hand-Hassel

ถ้าเราเขียนใหม่ ให้ pH = A, pKa = B และ Log ([RN] / [RNH+]) = C
จะได้ A = B + C
เมื่อพิจารณา C
จากสมการ

จะพบว่า ค่า [RN] จะเท่ากับ 0 เมื่อ [RNH+] ไม่แตกตัวให้เลย —> [RN] / [RNH+] = 0
และ [RN] จะมากที่สุด คือ เท่ากับ [RNH+] เมื่อ [RNH+] แตกตัวได้ทั้งหมด 100% –> [RN] / [RNH+] = 1
เนื่องจาก C = Log ([RN] / [RNH+]) จึงเข้ากันได้กับสมการ Y = Log x
( Y=C , x = [RN] / [RNH+] )
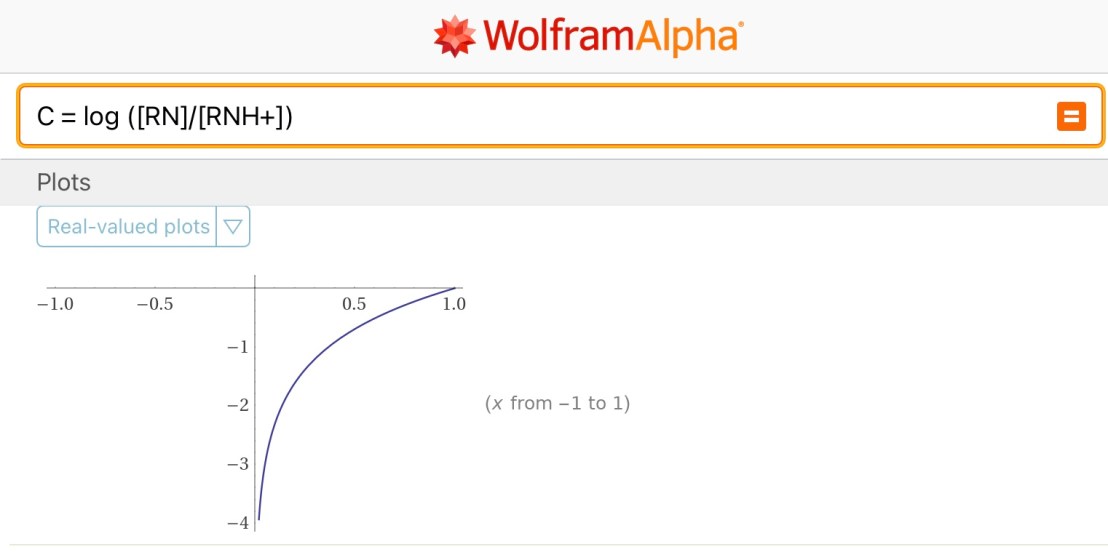
ค่า [RN] / [RNH+] ที่วิ่งระหว่าง 0 –> 1 จะทำให้ค่า C เป็น ค่าติดลบ เสมอ
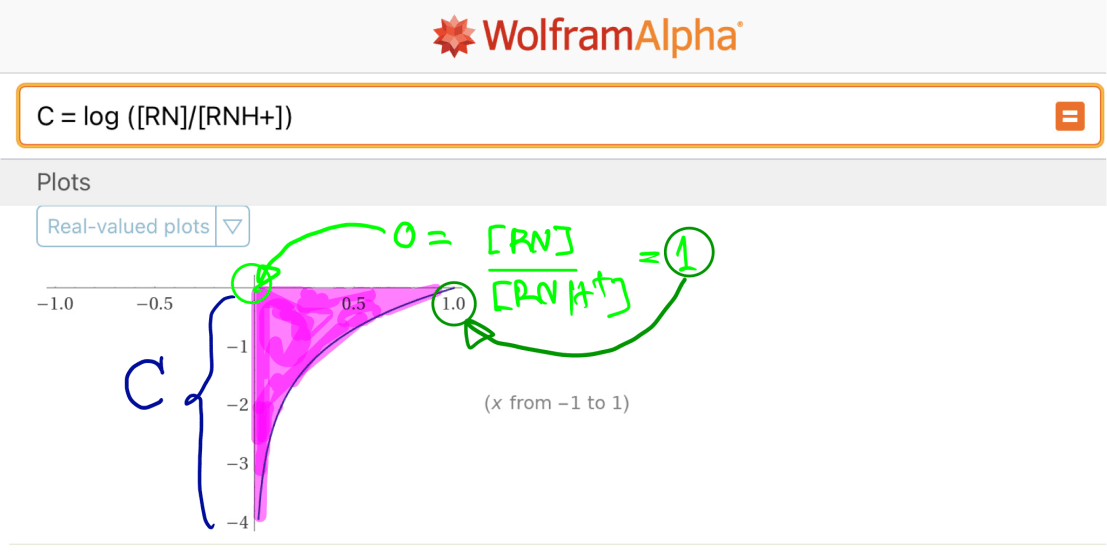
ดังนั้นถ้าให้ค่า A, B และ C เป็นจำนวนจริงบวกทุกค่า
จะได้สมการ A = B + C เป็น A = B – C
ถ้า A = B – C จะเกิดผล 2 ข้อ คือ A จะแปรผันตาม B
คือ ถ้า A มาก –> B จะมีค่ามากด้วย หรือ ถ้า A มีค่าน้อย –> B ก็จะน้อยด้วย
และ A < B เสมอ
กลับมาที่ สมการ
pH จะแปรผันตาม pKa และ pH จะมีค่าน้อยกว่า pKa เสมอ

กลับมาที่ตาราง
เราจึงพูดอีกแบบได้ว่า Articaine มีความเป็นกรดน้อยกว่า Mepivacaine นั่นเองครับ
หรือจะบอกว่า Bupivacaine เป็นเบสมากกว่า Articaine ก็ได้
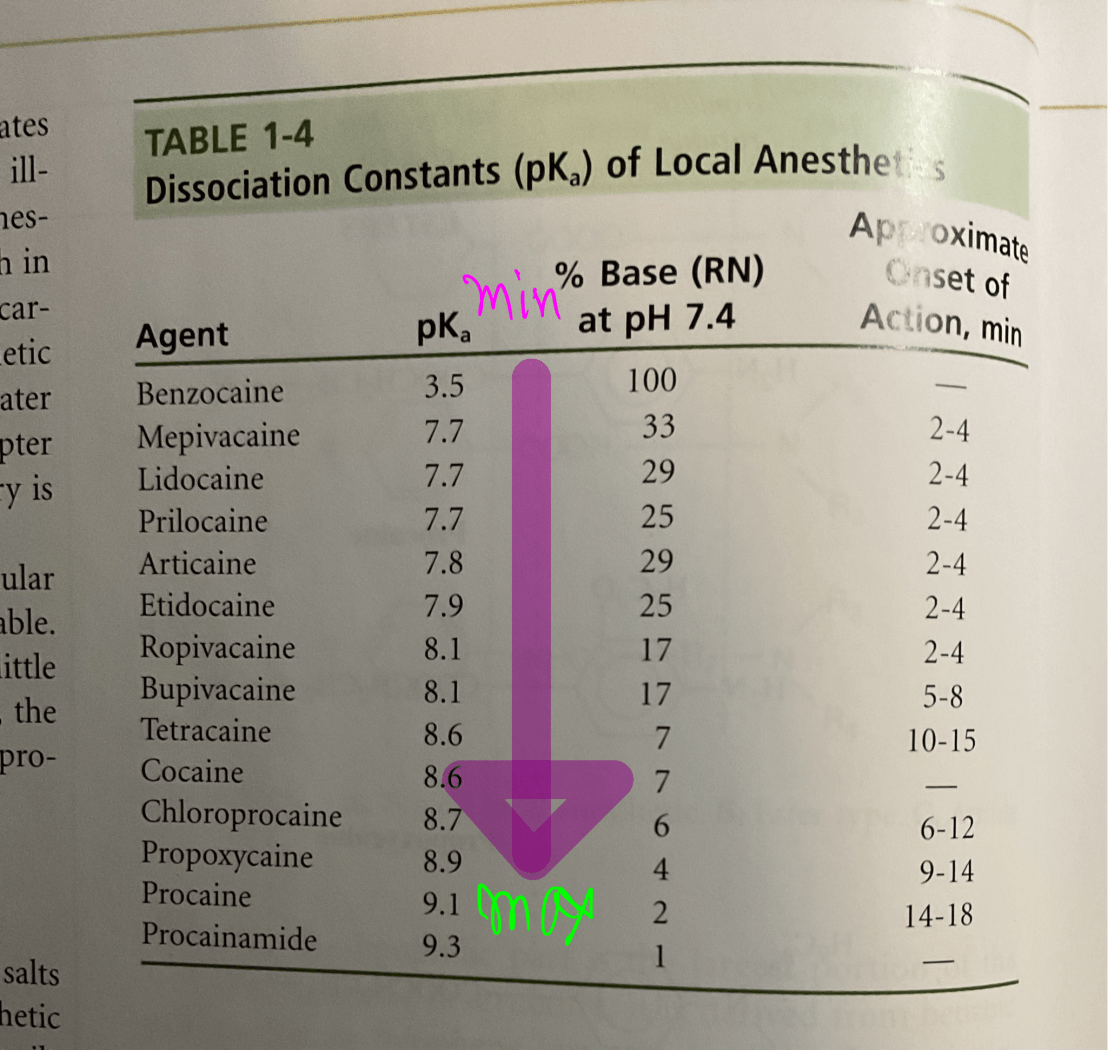
มองยาชาในตาราง ในมุมของ Acid-Base ของ B
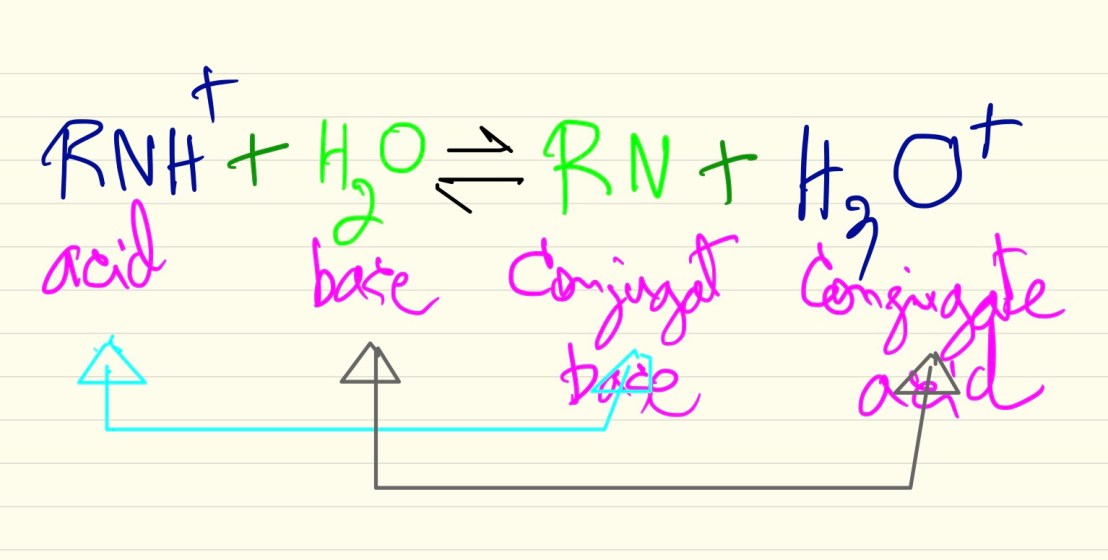
จากสมการการแตกตัวของยาชา

ถ้าเขียนเต็มรูปแบบ ตามทฤษฎีกรด-เบส ของ Brønsted-Lowry theory จะได้แบบนี้
คือ สนใจการให้และรับ Proton (H+)
RN คือ ยาชาที่แตกตัวจาก RNH+ หรือ พูดอีกอย่างว่า RN คือ คู่เบสของ RNH+ และเนื่องจากเป็น Buffer จึงมีสมดุลย้อนกลับ ว่า RNH+ คือ คู่กรด (ที่เกิดจากการรับ Proton) ของ RN นั่นเอง
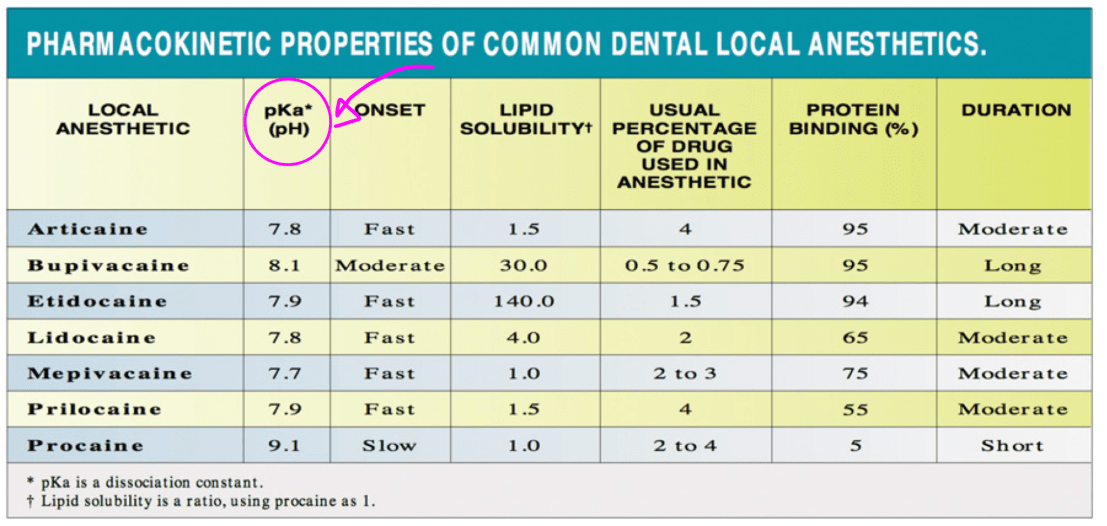
เพราะค่า pH แปรผันตาม pKa ถ้าไปอ่านเจอแบบนี้ ก็ไม่ต้องงงครับ
แต่ให้เข้าใจว่า ถึงมันจะแปรผันตามกัน แต่เป็นคนละค่ากัน ใช้อธิบายคนละเรื่องกัน คือ ตัวนึงอธิบายการแตกตัว ส่วนอีกตัว อธิบายการให้ H+ จากการแตกตัวนั้่น
จาก สมดุลของสมการ จะพบว่า ในสภาวะแวดล้อมที่เป็นกรดมากขึ้น สมดุลของสมการจะเป็นแบบนี้
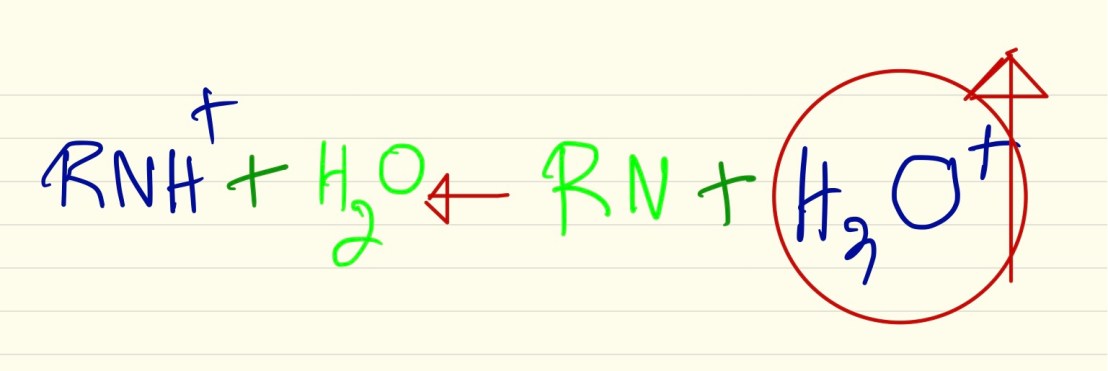
ยาชาที่มีความเป็นกรดมาก จึงใช้ในสถานการณ์นี้ไม่ดี (ถ้าไม่คิดถึง condition อื่นๆ ของ Pt)
ยาชาที่เหมาะ จึงเป็นยาชาที่มีความเป็นเบสสูง (pKa มาก ยิ่งดี)
คือ ถ้าเจอคนไข้มี Vestibular abscess ถ้ามี Mepi กับ Articaine ในคลินิก ให้เลือก Articaine แต่ถ้ามี Bupivacaine ให้เลือกใช้ Bupi แทน เป็นต้น
จบการอธิบายการใช้ Henderson-Hasselbalch equation ไว้เพียงเท่านี้
Ref:
2. https://todayinsci.com/H/Henderson_Lawrence/HendersonLawrence-Quotations.htm