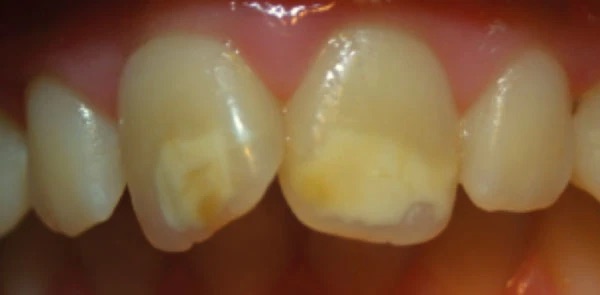
MIH ย่อมาจาก Molar Incisor Hypomineralisation
รูปแสดง MIH เป็น lesion ที่มีลักษณะ opaque และขอบเขต irregular บริเวณ #11,21
ปกติผมไม่ทำ pt เด็กเลย เรียกว่า ทิ้ง Pedo มานานมาก จนจำไม่ได้แล้วว่า ครั้งสุดท้ายที่ทำ pt เด็ก คือ เมื่อไร? นานจนจำความไม่ได้
จนมาวันนี้ อาจารย์เพื่อน ที่เป็นหมอ Pedo กรุณาส่ง link นี้มาให้ เพื่อช่วยทำ Questionnaire

ก็เริ่มทำโดยยังไม่รู้สึกอะไร แต่หลังจากผ่านหน้าแรก เข้าหน้าที่ 2 เท่านั้นแหละ ทำเอาผม shock ไปเลย เพราะไม่เข้าใจในสิ่งที่ถาม
หน้าที่ 2 เริ่มต้นด้วยข้อนี้
ที่ shock เพราะรู้สึกว่า นี่ความรู้ Pedo ของผม มันแย่ซะจน ไม่สามารถตอบแบบสอบถามทั่วไปของทันตแพทย์ได้แล้วเหรอนี่?
ในใจยิ่งทบทวนไปก็อายมาก ที่จบ D.D.S. แต่นอกจากจะ “ทิ้ง” pt เด็ก แล้วยังไม่เหลือความรู้ ไม่ได้ update ความรู้ Pedo เลย จนถึงขนาดไม่สามารถตอบแบบสอบถามพื้นๆ แบบนี้ได้แล้ว

บทความนี้จึงเกิดจาก ความรู้สึกผิดและอายเป็นพื้นฐาน และ ใช้เวลาอ่าน Paper เรื่อง MIH เพียง 2 ชิ้นเท่านั้น (หมายความว่า รู้เรื่อง MIH ในขอบเขตจำกัดของ Paper ที่อ้างอิงเท่านั้นครับ) เพื่อให้มีความรู้พอที่จะเข้าใจ MIH และทำแบบสอบถามชุดนี้ได้
โดยสรุป
MIH ( Molar incisor hypomineralisation ) “ไม่ใช่” โรค caries ครับ แต่เป็น ความผิดปกติของ Ameloblast ในการสร้างชั้น Enamel ที่เกิดขึ้นในฟันบางซี่เท่านั้น (คือ 1st molar กับ incisor)
โดยแรกเริ่ม เทอม MIH เริ่มใช้ในปี พ.ศ. 2544 โดย Dr.KL Weerheijm
ชื่อ Dr. Weerheijm ออกเสียงตามนี้
MIH ในตอนแรกสุด define ว่า เป็นความผิดปกติของการเกิด Hypomineralisation ที่มาจาก systemic origin เกิดกับ ซี่ 6 (ตั้งแต่ 1-4 ซี่) และกระทบไปถึง incisor (ที่เกิดการพัฒนาในช่วงเดียวกัน) จึงเป็นที่มาของ Molar และ Incisor ที่เกิด Hypomineralisation
MIH ไม่ใช่โรคฟันผุ ไม่ใช่โรคทาง Genetics แต่เป็นโรคที่เกิดในระหว่างการ develop ของ enamel
ในช่วงที่ผมเรียนในคณะ Chrological age และ Dentition age จะอิงกับ Ubelaker ดังภาพ ทั้งภาค Oral med และ Ortho จะใช้ Ubelaker ในการสอน
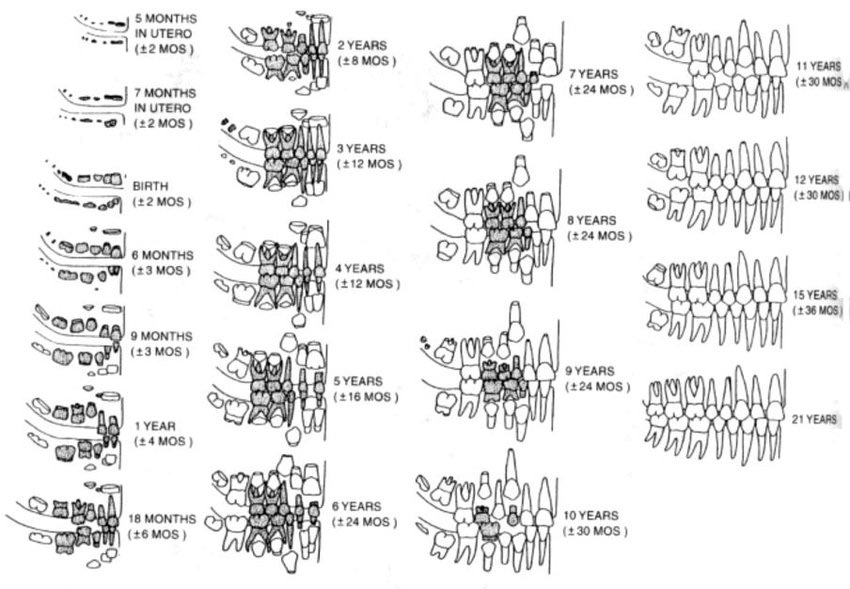
แต่ปัจจุบัน เรารู้แล้วว่า Ubelaker dental chart เพี้ยนมาก และจะใช้ London atlas ในการอ้างอิงเป็นหลัก
ชื่อว่า London แต่ใช้อ้างอิง Dentition age ในคนไทยได้ดีมากครับ ( error ระดับ +/- ความแตกต่างของอายุปฎิทิน กับ อายุการขึ้นของฟัน น้อยกว่า 1 ปี)
รูปแสดง London atlas จะเห็นว่า 1st Molar และ Incisor มีการ calcify Crown ที่คาบเกี่ยวช่วงอายุกัน
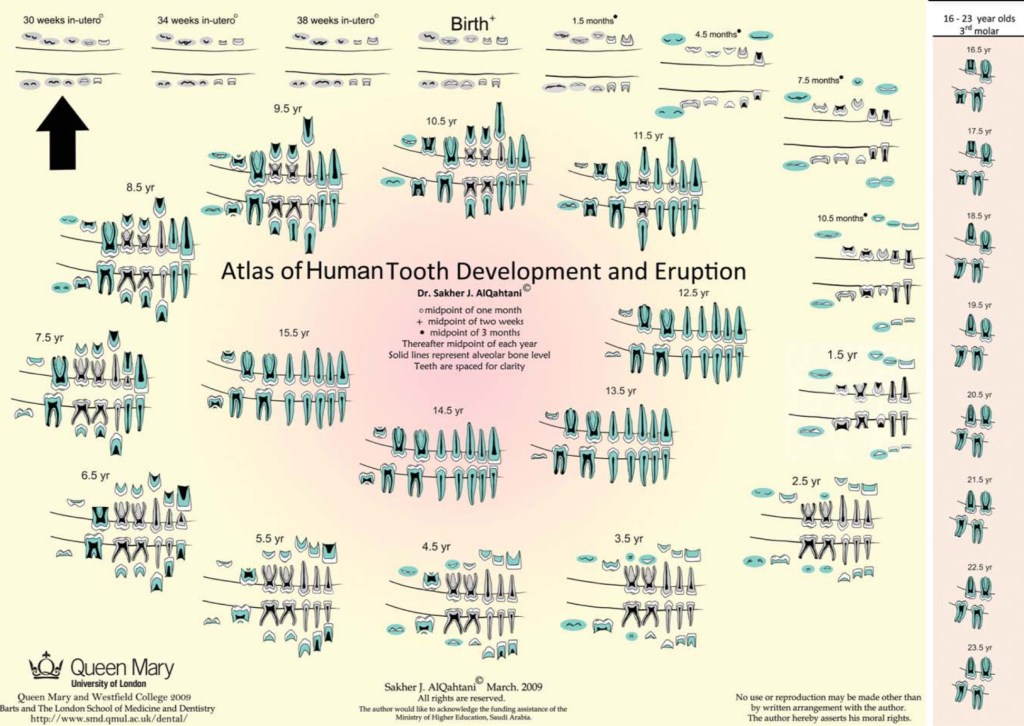
ขยาย London atlas ใน pt อายุ 5 ปี
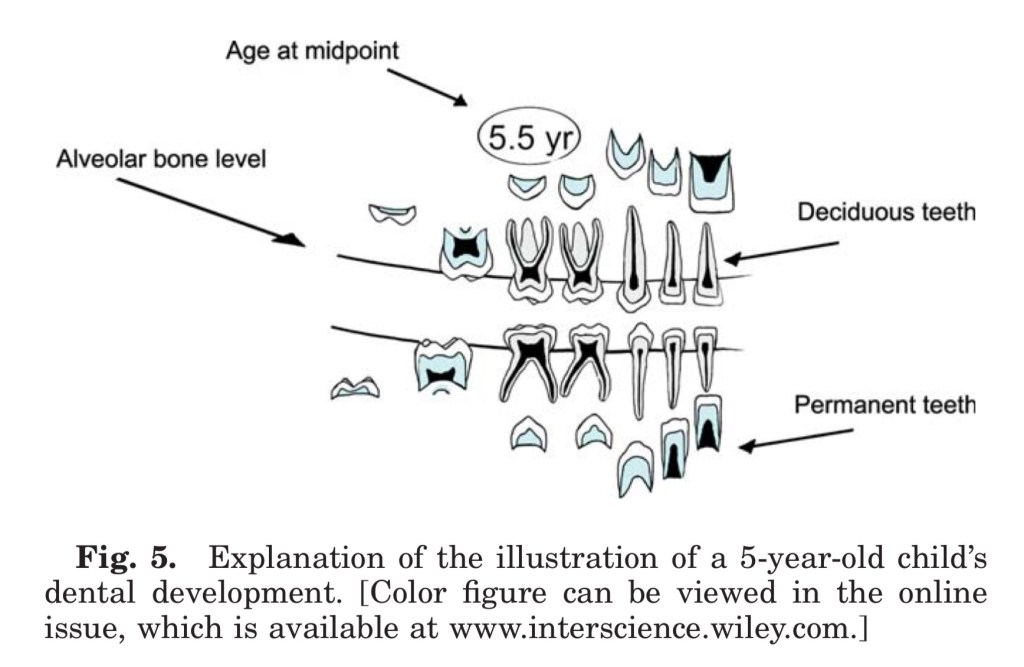
ระยะการ Calcify ของ Incisor และ ซี่ 6 ที่มี Overlap
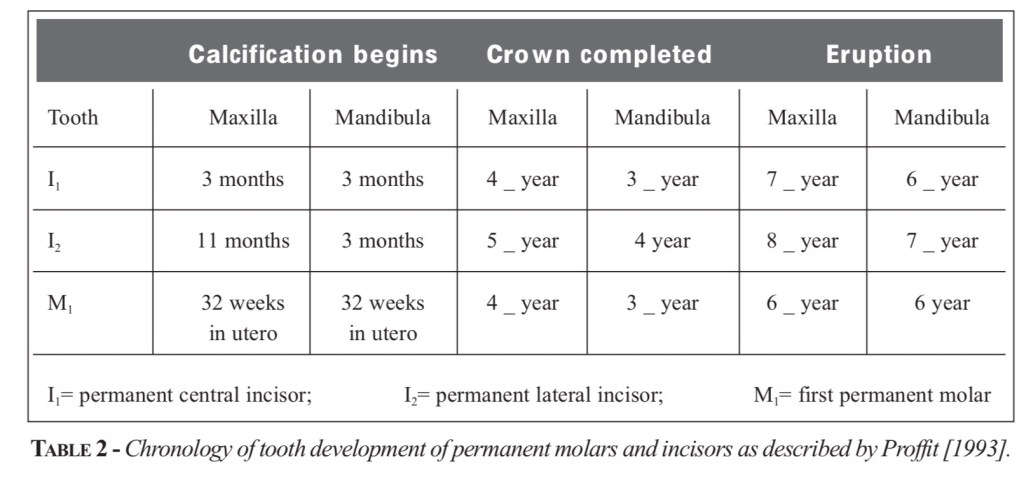
MIH ไม่ใช่ฟันผุ แล้วเราจะ diff Dx จาก caries หรือ ความผิดปกติของโรคที่เกิดกับ enamel ตัวอื่นได้ยังไง ?
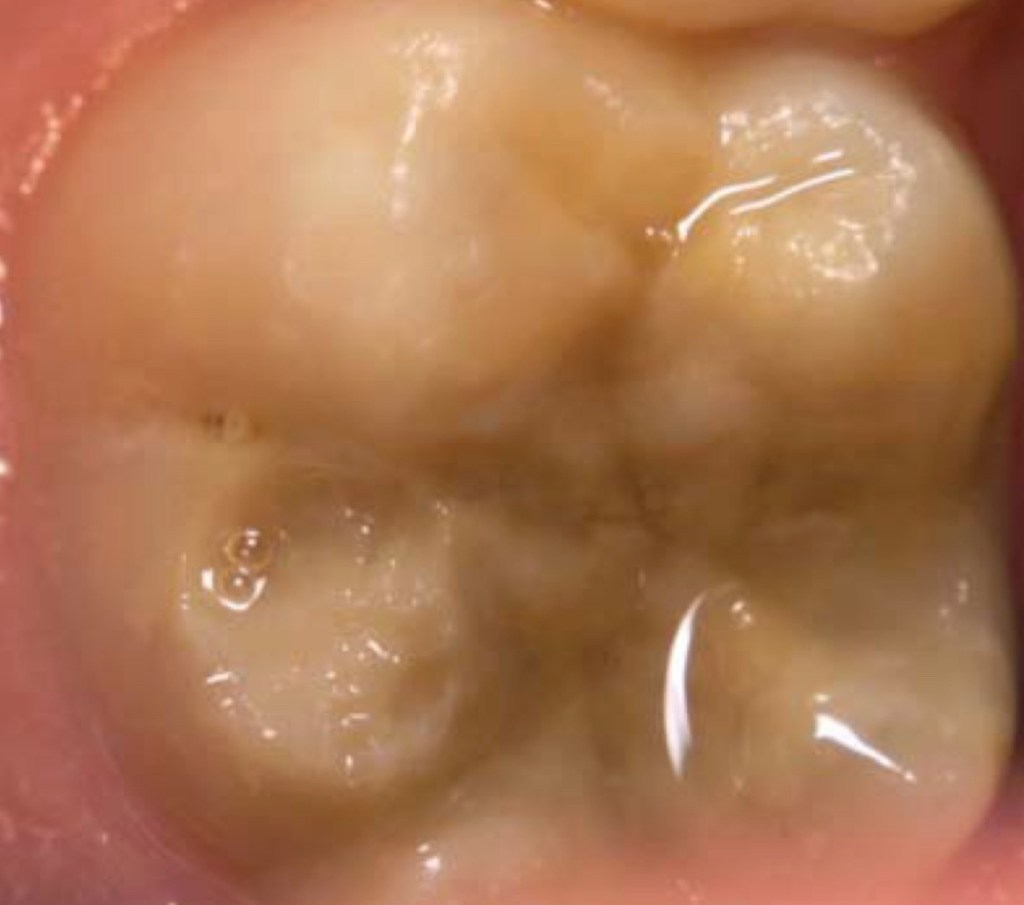
- diff Dx จากฟันผุ จะเห็นว่า ถึงแม้ MIH ในรูป คล้าย White spot lesion caries แต่ลักษณะที่ ไม่มี plaque คลุมบริเวณนี้อยู่ จึงไม่ใช่ caries
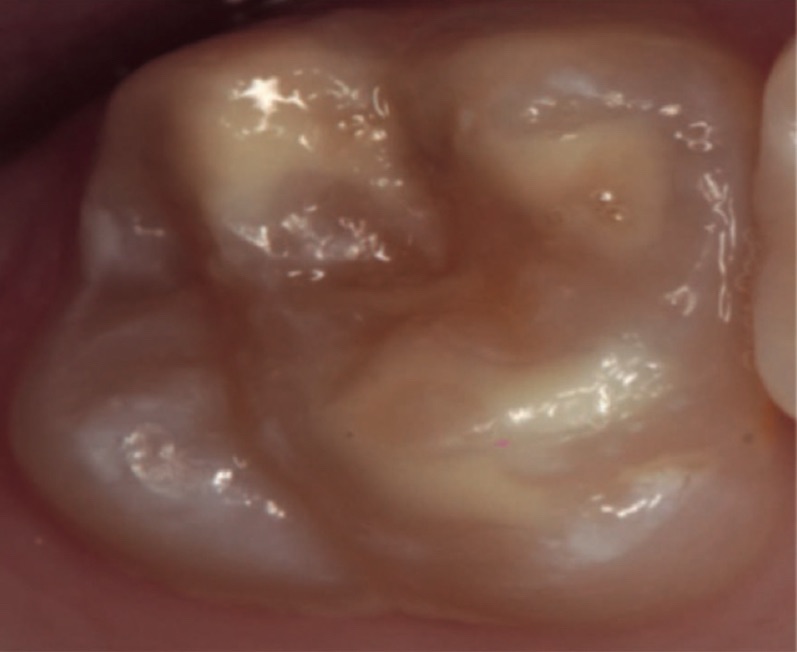
ลักษณะขาวขุ่นของ Opaque enamel ที่เห็นใน 1st molar คือ MIH
2. แยกจาก Fluorosis ได้จาก Fluorosis จะเกิดในฟันทั้งปากในรูปแบบ symmetry และ bilateral pattern ขณะที่ MIH จะเกิดแบบเฉพาะบางซี่ และ ไม่ sym
3. แยก MIH จาก Enamel Hypoplasia ได้จาก ใน hypoplasia ชั้นความหนาของ enamel จะบาง และขอบ lesion regular, smooth
Enamel Hypoplasia เกิดจากการรบกวน Ameloblast function ในระยะ secretory phase นำมาสู่ ความผิดปกติในการสร้าง enamel matrix ทำให้เมื่อ eruption เราจะพบชั้น enamel ที่บางลง และความผิดปกติเริ่มในชั้น superficial
แต่ MIH stage ของ enamel matrix formation จะปกติ ทำให้ตอน eruption lesion จะมีขอบ irregular จากฟัน molar เริ่มรับแรง และ break down ทำให้บางครั้ง เกิดความสับสนกับ Enamel Hypoplasia
ลักษณะ Classic ของ MIH คือ effect ที่ซี่ 6 และ Upper incisor ด้วย ( case ที่พบ Lower incisor ก็มี แต่น้อยกว่ามาก)
รูปแสดง MIH ที่เกิดใน Lower incisor
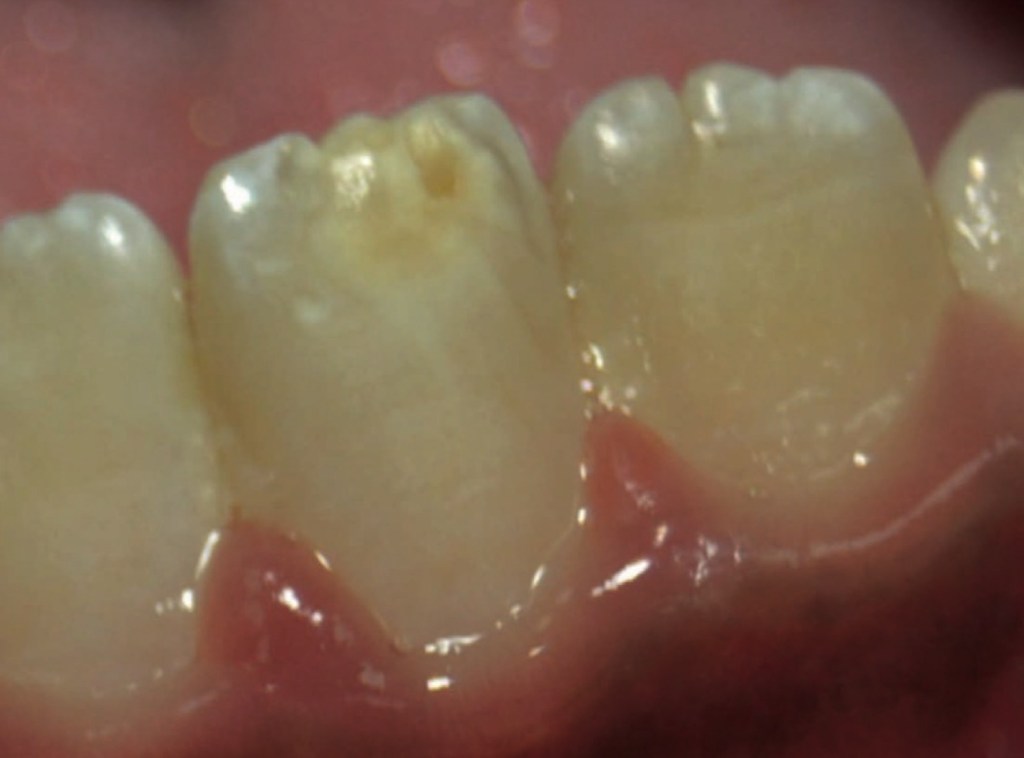
4. แยกจาก Amelogenesis imperfecta อันนี้ง่ายมาก เพราะเป็น Genetic และ effect ฟันทุกซี่ diff จากการตรวจ และ Familial Hx
Ok เรารู้ว่า MIH เกิดจากความผิดปกติในการสร้าง enamel เฉพาะที่ และ กระทบฟันบางซี่ เท่านั้น แล้ว ปัญหาของ MIH คืออะไร ?
เรารู้ว่า lesion ที่ขาวทึบ (หรือ เหลือง-น้ำตาล ถ้า severe ขึ้น) ของ MIH เกิดจากความผิดปกติการพัฒนาการในช่วงสร้าง enamel ที่เกิดจาก systemic factor ที่เข้ามารบกวนการ calcify ของ Ameloblast cell แต่สาเหตุคือ systemic factor ใด? ยังไม่สามารถบอกแบบเจาะจงได้
Opaque area ที่เกิดในชั้น enamel เกิดจากการหักเหของแสงเมื่อตกกระทบ แล้วทำให้ชั้นนี้ขุ่น —> แสดงว่า ความใส ( translucency ) ในชั้นนี้ ถูกทำลาย หรือ ทำให้เกิดรูพรุน
การสร้าง enamel ประกอบด้วย Secretory phase เป็น การเกิด mineral deposition ในชั้นความหนาของ enamel ทั้งหมด แล้วตามด้วย Maturation phase
ในช่วงท้ายๆ ของ Maturation phase จะมีการดึง organic material และ ดึงน้ำ ออกจากชั้น enamel เพื่อแทนที่ด้วย mineral ที่ influx เพิ่มเข้าไป การเกิดการรบกวนในขั้นตอนนี้ ทำให้ enamel เกิด opaque ที่เห็นได้ในทางคลินิก
ในทาง Histo คือ MIH เกิดจากการมีสิ่งเข้าไปรบกวน Ameloblast ใน Maturation phase นั่นเอง (ต่างจาก Amelogenesis imperfecta เกิดจากการรบกวนใน Secretory phase)
จากรูพรุนของชั้น enamel —> นำมาสู่การ break down และ fx ของ area นี้ โดยเฉพาะบริเวณของ tooth surface ที่เป็น stress bearing area –> เกิด caries , เกิด Hypersensitivity (ถ้าเกิดบริเวณ labial ของฟันหน้าบน ที่เห็นชัด นั่นคือ ปัญหาทาง esthetic ยิ่งเด็กที่อยู่ในช่วงเข้าสู่วัยรุ่นตอนต้น —> นำมาสู่ปัญหาการ bully จากเพื่อนในโรงเรียน จนมี effect ทางด้านจิตใจ (ทำเป็นเล่นไปนะ สมัยนี้))
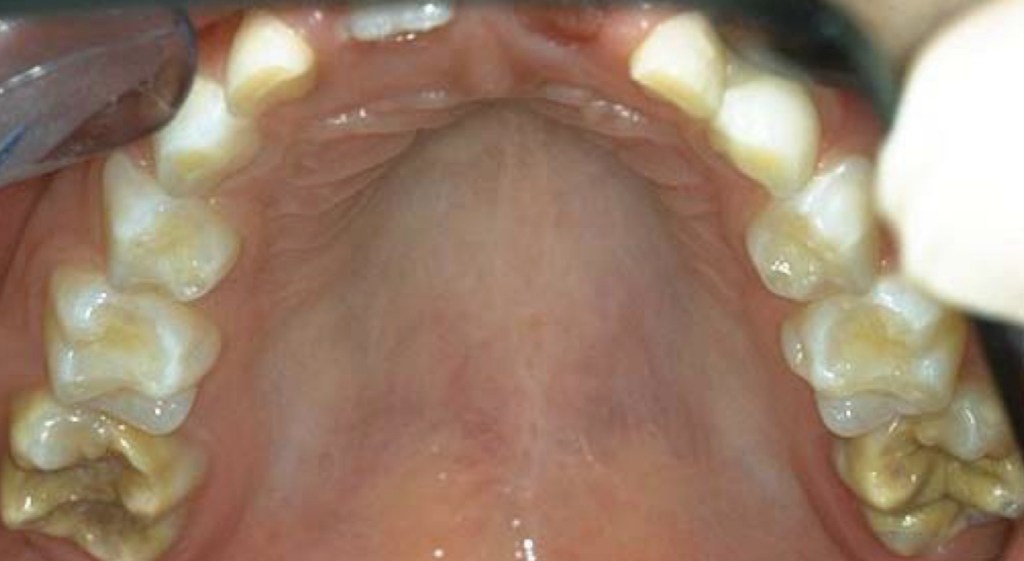
รูปนี้ แสดง MIH ที่เกิดใน #16, 26 อย่าสับสนว่า มันเกิดแบบ symmetry เพราะจะเห็นว่า #16 เกิดการผุเรียบร้อยแล้ว แต่ #26 ยังไม่ผุ แต่เป็น yellow opaque อยู่ (คือตอน Eruption #16 ก็เหมือน 26 ครับ แต่หลังจาก pt เริ่มใช้งานเจอ occlusal load บริเวณ enamel ที่ hypomineralise มีรูพรุนก็ fx แล้วเกิด caries)
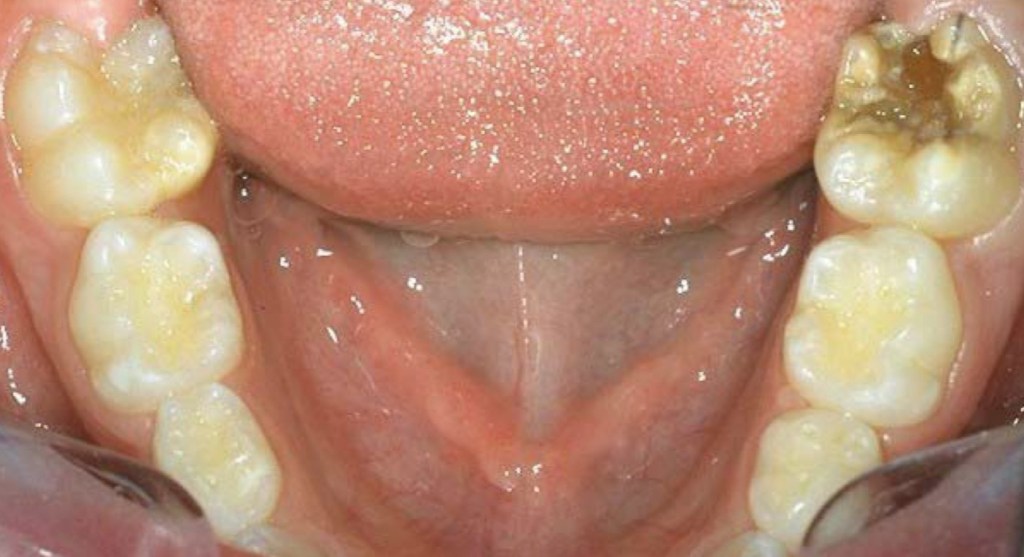
ใน pt คนเดียวกัน ฟันล่างพบ #36 MIH แต่ 46 ปกติ —> นั่นคือ Asymmetry
แต่จากการที่ MIH เกิดที่ #26 ด้วย และ #16 ด้วย ทั้ง 2 ข้าง ซ้ายและขวา นั่นคือ เกิด MIH แบบ contralateral ซึ่งแสดงถึง severity ของ MIH ที่ degree สูงขึ้น
มีคนพยายามแบ่ง Severity ของ MIH เป็น Classification
จาก Definifion ของ MIH ตอนเริ่มต้นในปี พ.ศ. 2544 ที่จำกัดในฟัน molar และ incisor เฉพาะในฟันแท้ จนถึงปัจจุบัน MIH ยังไม่เปลี่ยนชื่อ แต่ครอบคลุมถึง lesion ลักษณะเฉพาะนี้ที่เกิดขึ้นใน ฟันน้ำนม ( ซี่ E ) และ ฟันแท้ซี่อื่น เช่น Canine (บริเวณ cusp tip ) ด้วย
เทอมที่ใช้เฉพาะของซี่ E คือ HSPMs (Hypomineralised Second Primary Molars)
ในเด็กที่ตรวจแล้วเจอ HSPMs สามารถใช้ทำนาย และเฝ้าระวังการเกิด MIH ในเวลาต่อมาได้ แต่การตรวจไม่เจอ HSPMs ไม่สามารถ r/o ได้ว่า จะไม่เกิด MIH อีกในเด็กคนนั้น ในอนาคต

ความสำคัญของ MIH คือ เราจัดการมันได้ ถ้าเรารู้จัก และ monitor
จากรูป #36 บริเวณ Disto-buccal cusp
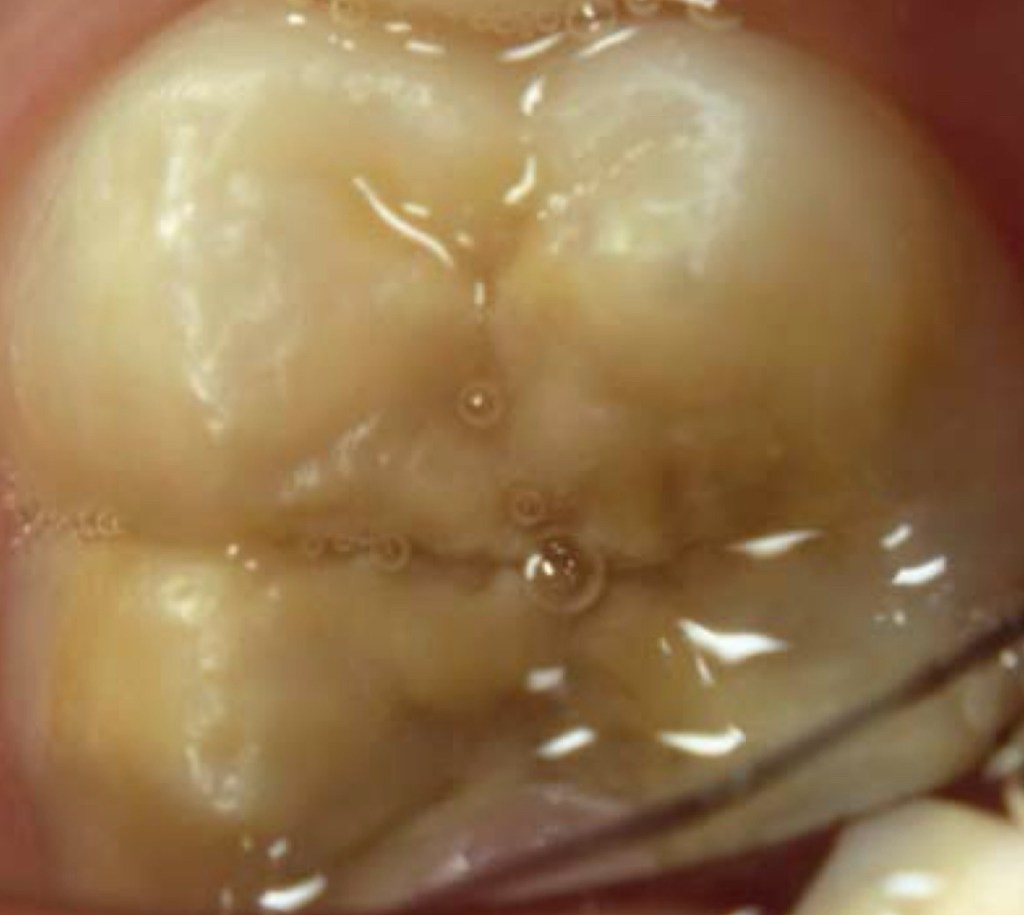
รูปแสดง ฟันซี่เดิมในอีก 3 เดือนต่อมา
แล้วเราจะจัดการยังไงกับ MIH ?
ที่ผมนึกได้ คือ ใช้ Oper เข้าไปจัดการเป็นหลัก และถ้าเก็บไว้ไม่ได้ ก็ Pulp Rx และ Extraction ในกรณีที่หนักสุด
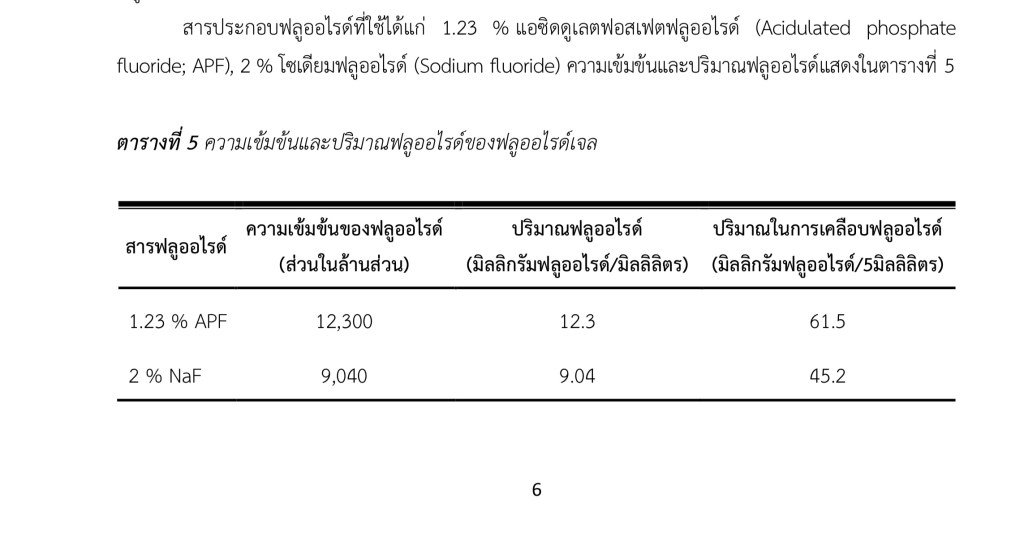
ถ้าเริ่มจากมาตรการเบาสุด เจอ MIH ในระยะเริ่มแรกจริงๆ และ enamel ยังไม่ break down คือ ใช้การ Prevention ด้วยการ Remineralise กลับไป แต่การ apply Fluoride อย่างเดียว ไม่พอที่จะจัดการกับ MIH เพราะ F product จะ Remineralise เฉพาะ Surface เท่านั้น แต่ MIH เกิด Hypomineralise ที่ deep กว่านั้นมาก
อย่างน้อยๆ ต้องใช้ CPP-APP product (Casein Phosphopeptide Amorphous Calcium Phosphate) ครับ เช่น Tooth Mousse ของ GC หรือ MI Paste Plus ( 10% CPP-APP + 0.2% NaF)
Contra ของ CPP-APP product คือ เด็กที่แพ้ milk protein
อีกตัวที่ใช้ได้ คือ Enamelon Treatment Gel ของ Premier Dental มี ACP + F 970 ppm จะ Remineralise ได้เทียบเท่า F product ที่มี 5,000 ppm
ยาสีฟันที่มีส่วนประกอบของ Novamin (DGSK) เป็น Bioglass particle size 18 micron เพราะเป็น toothpaste จึงใช้ได้บ่อยกว่า Tooth Mousse ในระยะยาว พบว่า Remineralise ได้ดีกว่า Tooth Mousse
ถ้า lesion เป็นมากขึ้นมาอีก ก็ Oper มาตรการหนักขึ้น เป็นการทำ Sealant แต่การ Sealant ในฟัน MIH จะต่างจากในฟันปกติ เพราะระดับการ Hypomineralise รุนแรงกว่ามาก
ถ้าจะใช้ Sealant ในฟัน MIH มีคำแนะนำให้ใช้ DBA ร่วมด้วย โดย bonding ก่อน Sealant หรือ Pretreat enamel ก่อน Sealant ด้วยการทา Deproteinising agent คือ 5% NaOCl หรือ Papain-based papacarie gel ทา 60 s ก่อน etch เพื่อเพิ่ม bond strength
แต่ถ้าความเสียหายมากกว่า Sealant ก็ใช้ Oper เป็น GI หรือ Composite
มีข้อสังเกตอีกอย่างคือ ในฟัน molar ที่เป็น MIH จะทำให้ชาด้วย LA ยากกว่าฟันปกติ มีคำอธิบายว่า เพราะ enamel ที่ MIH effect เป็นเกราะป้องกันที่แย่มาก ทำให้ pulp protect ได้ไม่ดี จึงพัฒนาเป็นการเกิด Hypersensitivity ในฟันซี่นั้น การใช้ LA จึงต้องใช้เทคนิกการฉีดหลายวิธีร่วมกันมากขึ้น (เหมือนใน Adult)
มีคำแนะนำให้ใช้ สารลด Hypersense ก่อน visit ที่จะมา Oper โดยเลือกใช้ได้หลายแบบ ตั้งแต่ Fluoride vanish ก่อน หรือ ใช้ GI เป็น interim restoration คือ ทำเป็น 2 step restoration technique
การจัดการด้วย Oper กับฟัน molar ที่เป็น MIH
เริ่มเบาๆ ได้ตั้งแต่ ทำ Resin infiltration ด้วย Icon (DMG)
ซึ่งประกอบด้วย Icon etch ด้วย 15% HCl –> Icon dry ด้วย 99% Ethanol –> Icon infiltrant ด้วย Methacrylate-based resin
จะเห็นว่า การ Etching ใน Resin infiltration นั้นรุนแรงกว่าที่เราใช้กันปกติมาก กรดจะ etch ได้ deep กว่า และ การ Infiltrate ต้องแน่ใจว่า resin สามารถเข้าไปในชั้นที่ลึกนั้นได้เพียงพอ เวลาในการทำงานจึงมากกว่าที่เราทำกันใน filling ทั่วไป
ใน lesion MIH ที่ความเสียหายมากขึ้น ตอนนี้ Oper จะเข้าสู่การ filling ตามปกติ และจากขอบ lesion ที่ irregular การออกแบบ cavity prep ทำได้ยากกว่า caries ปกติ วัสดุที่เหมาะสมจึงจำกัดในกลุ่ม GI, RMGI, Composite เท่านั้น
ถ้า lesion damage มากขึ้นไปอีก —> SSC
ระดับต่อมา คือ การเลือก Proper Pulp Rx
จนถึงมาตรการสุดท้าย ถ้า Restore ไม่ได้ ก็คือ Extraction
การ Extract ฟันซี่ 6 ก็ใช้การพิจารณาคล้าย Serial extraction ครับ คือ ต้อง film เพื่อดู ซี่ 7 จากความรู้เดิมว่า ซี่ 7 จะเกิด Intra-osseous migration มาแทนที่ซี่ 6 ได้ดีที่สุด ระยะที่เหมาะสม คือ การถอนซี่ 6 ในขณะที่ film แล้ว ซี่ 7 ยังกำลังทำ Root formation และมี Follicle ครอบคลุมอยู่อย่าง complete
ความสำเร็จในการแทนที่ ซี่ 6 ด้วย ซี่ 7 จะเกิดได้ดีมากๆ ใน max > mand (ตัวเลขคือ 94% vs 66%)
ถ้าทำนาย หรือ monitor ได้ว่า การเคลื่อนมาแทนที่ไม่ดี —> ใช้ Ortho เข้ามาช่วย
รูปแสดง การใช้ Resin infiltration ด้วย Icon infiltration
ข้อบ่งชี้ในการใช้ จริงๆ คือ เพื่อจัดการกับ White spot lesion caries (ไม่ใช่ MIH)
ความรู้พื้นฐานคือ refractive index ของ enamel = 1.62 และ ของ resin infiltrant = 1.52 ทำให้เมื่อทำเสร็จแล้วความ Opaque ของ enamel กลับมาใกล้เคียงค่าปกติ
แต่ข้อจำกัดของเทคนิคนี้ คือ ไม่เหมาะกับ MIH ที่เป็น mild degree เพราะ damage เกิดใกล้ Surface มากเกินไป ในขณะที่ resin infiltration จะเข้าไปแก้ refractive index ที่เข้าไปลึกกว่านั้น
การทำ Etching ใน Incisor MIH ต่างจาก White spot lesion ที่ของฟัน MIH ต้องใช้ Etching cycle หลายรอบ และ ใช้เวลามากกว่า
ในบาง case ที่ damage เข้าไปลึกมาก การช่วยให้ resin infiltrate ได้ดีขึ้น โดยการ sandblast ที่ผิว ช่วยได้
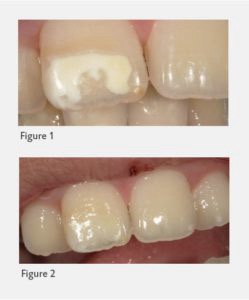
ถ้ายังไม่ใช้ Resin infiltration แต่เลือกใช้ เพียง Microabrasion (18% HCl หรือ 37.5% Phosphoric + pumice) ให้พิจารณาว่า จะกำจัดได้เฉพาะบริเวณ Superficial เท่านั้น ซึ่งมักไม่ได้ผลกับ MIH (ซึ่ง deep กว่านั้น)
ยกเว้นว่า Incisor เป็น MIH ระดับน้อยจริงๆ อาจตัดสินใจใช้ Microabrasion + CPP-APP product ร่วมด้วยที่บ้าน แล้ว F/U เป็นระยะครับ
กรณีต้องการแก้สีฟันหน้า ที่เกิด Opaque เพียงอย่างเดียว สามารถใช้ 10% Carbamide peroxide gel ได้ โดยร่วมกับ CPP-APP Tooth Mousse
ส่วนใน case ที่สีฟันหน้าเป็น lesion แบบ yellow-brown stain สามารถ bleach โดยการใช้ 37% Phosphoric acid apply 60 s —> 5% NaOCl เพื่อ bleach 5-10 min —> Re-etch —> ปิดด้วย Clear Sealant หรือ DBA ผลลัพธ์คือ yellow-brown stain จะกลายเป็น white mottled appearance ซึ่ง esthetic ดีกว่า เรียก technic นี้ว่า Etch-bleach-seal technic
ถ้า lesion ลุกลามมากกว่าจะ filling ได้ —> Composite veneer, Porcelain veneer (ข้อแตกต่างในการพิจารณาที่จะทำ อยู่ที่ขีดจำกัดด้านอายุของ pt เส้นแบ่งอย่างคร่าวๆ จะอยู่ที่ 18 ปี จึงจะพิจาณาทำแบบ Permanent ได้)
ref:
- https://www.nature.com/articles/sj.bdj.2018.814
- https://forms.office.com/Pages/ResponsePage.aspx?id=yCT26sSglUGH0kQ-XXUWzd5bN3l4BsFJhwOoHIwaD9BUN1g5Uk9OM0hNUkhRNEtUSkIzR0tHRVY5Ny4u
- https://pubmed.ncbi.nlm.nih.gov/14529330/
- https://www.researchgate.net/figure/Fig-No27-Grafico-de-erupcion-dental-en-nativos-norteamericanos-Dh-Ubelaker-1994_fig8_323734165
- https://www.tandfonline.com/doi/full/10.1080/00450618.2022.2040588
- https://www.dentalage.co.uk/wp-content/uploads/2014/09/alqahtani_sj_et_al_2010_atlas_of_tooth_development1.pdf
- https://dmg-connect.com/articles/resin-infiltration-in-the-treatment-of-mih-lesions-in-anterior-teeth-in-pediatric-patients/